
 English
English
 French
French
Histiocytose X chez un jeune fumeur
Histiocytosis X in young smoker
A. Sqalli Houssaini, I. Nassar, H. Malajati, L. Hammani, A. Ajana, F. Imani
Service de Radiologie. CHU Ibn Sina. Rabat, Maroc
Corresponding author
A.Sqalli Houssaini
Service de Radiologie. CHU Ibn Sina. Rabat. Avenue Imam-Ali, Résidence Zeryab n 7, Appartement n 5, V.N., Fès, Maroc
E-mail: assmae26@hotmail.com
DOI: 10.12699/jfvp.2.3.2011.37
ABSTRACT
The pulmonary histiocytosis X is rare pathology. The exact frequency is unknown. In most cases the pulmonary lesions is isolated. This pathology occurred in young adults with a peak age between 20 and 40. Between 90 to 100% of patients are smokers. Some cases have been reported frequently after radiotherapy or chemotherapy for Hodgkin's lymphoma in particular.
The clinical presentation of histiocytosis X is polymorphic. In the fourth case was discovered incidentally by routine radiography. Patients present with respiratory signs, dominated by a dry cough. These signs may be associated with general symptoms (fever, fatigue, night sweats and weight loss). In some cases, the diagnosis is made during a spontaneous pneumothorax.
In this paper, we present a case of histiocytosis X in its evolutive cystic forme occurred in a young smoker who had a chronic dry cough without other associated clinical signs. Histiocytosis X was diagnosed with chest CT high resolution which showed multiple formed cystic within thin and irregular alveolar walls, variable size and form and without lobar predominance. The pathology was confirmed by histological study.
KEYWORDS: histiocytosis X, dry cough, pneumothorax, cystic
RÉSUMÉ
L’histiocytose X pulmonaire est une affection rare. La fréquence exacte reste inconnue. Dans la plupart des cas l’atteinte pulmonaire est isolée. Elle est survenue chez le sujet jeune avec un pic d’âge entre 20 et 40 ans. Entre 90 à 100% des malades sont des fumeurs. Certains cas ont été rapportés souvent après radio ou chimiothérapie pour lymphome notamment hodgkinien.
La présentation clinique de l’histiocytose X est polymorphe. Dans un quart des cas la découverte est fortuite par la radiographie systématique. Les patients se présentent avec des signes respiratoires, dominées par une toux sèche. Ces signes peuvent être associés à des signes généraux (fièvre, asthénie, sueurs nocturnes et amaigrissement). Dans certains cas, le diagnostic se fait à l’occasion d’un pneumothorax spontané.
Dans cet article, nous présentons un cas d’histiocytose X dans sa forme évolutive kystique survenue chez un jeun fumeur qui présentait une toux sèche chronique, sans autres signes cliniques associés. L’histiocytose X a été diagnostiquée grâce à la TDM thoracique en haute résolution qui montrait les multiples formations kystiques à paroi fine irrégulière, de taille et de forme variables sans prédominance lobaire. La maladie a été confirmée par la biopsie pulmonaire avec l’analyse histologique.
MOTS CLES: histiocytose X, toux sèche, pneumothorax, kyste
OBSERVATION
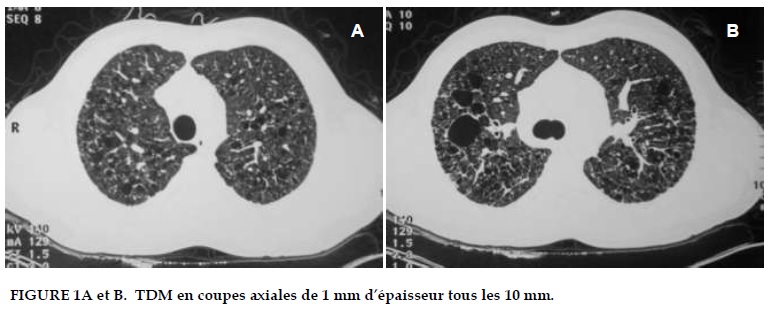
Il s’agit d’un jeun homme de 37 ans fumeur, qui présente une toux sèche depuis un mois, sans fièvre et sans altération de l’état général. Une radiographie thoracique puis une TDM thoracique en haute résolution ont été réalisées (Figure 1, 2).
- Quel est votre diagnostic ?
- TDM en haute résolution (Figure 1, 2)
DIAGNOSTIC
Histiocytose pulmonaire X dans sa forme évolutive kystique.
La TDM thoracique en haute résolution objective de multiples formations kystiques à paroi fine irrégulière, de taille et de forme variables sans prédominance lobaire (Figure 1, 2). Ces kystes sont centrolobulaires, certains sont isolés d’autres jointifs ou confluents par endroit. Il s’y associe une augmentation de la taille des artères pulmonaires en regard.
Le diagnostic d’hystiocytose X a été évoqué sur la clinique (sexe masculin), la taille variable des kystes, et de l’épaisseur de paroi, ainsi que l’absence de prédominance de siège.
La biopsie a confirmé le diagnostic de l’histiocytose X.
DISCUSSION
L’histiocytose X pulmonaire est une affection rare [1-3]. La fréquence exacte reste inconnue (3 à 5% des pneumopathies infiltratives diffuses) [1, 3, 4]. Dans plus de 85% des cas l’atteinte pulmonaire est isolée [5]. Elle affecte le plus souvent le sujet jeune avec un pic d’âge entre 20 et 40 ans.
Le sexe ratio est de: home/femme = 1,5 /1 [1, 3, 5]. 90 à 100 % des malades sont des fumeurs. Certains cas ont été rapportés souvent après radio ou chimiothérapie pour lymphome notamment hodgkinien [1, 5].
Sur le plan histopathologique ces affections ont en commun l’infiltration des tissus par des histiocytes atypiques organisés en granulomes [1, 3, 5, 6]. Ultérieurement, il a été montré que les histiocytes étaient similaires aux cellules de Langrhans, ce qui est à l’origine de la dénomination actuelle histiocytose Langrhansienne [3, 5].
La présentation clinique de l’histiocytose est polymorphe. Dans 25% des cas la découverte est fortuite par la radiographie systématique [1, 3]. Dans 2/3 des cas les patients se présentent avec des signes respiratoires fonctionnels, dominées par une toux sèche, une dyspnée d’effort reste moins fréquente. Ces signes peuvent être associés à des signes généraux (fièvre, asthénie, sueurs nocturnes et amaigrissement). Dans 10 à 20 % le diagnostic se fait à l’occasion d’un pneumothorax spontané [3, 5, 7].
L’examen physique est souvent normal en dehors des manifestations extra-thoracique (pneumothorax, atteinte costale, et au stade du cœur pulmonaire chronique).
A la radiographie thoracique [1, 5, 8, 9], les images sont corrélées aux aspects anatomopathologiques. L’évolution de la maladie se fait en trois stades:
Stade I
Phase exsudative caractérisée par une alvéolite transitoire. Il s’agit soit de plages d’hyperdensité en verre dépoli ou de lésions alvéolaires à type œdème pulmonaire. L’observation de ce stade est exceptionnelle car il est transitoire.
Stade II
Phase granulomateuse avec aspect nodulaire : La plus fréquemment rencontrée. Il s’agit soit de micronodules, de nodules ou d’opacités réticulonodulaire. Les images sont habituellement bilatérales et symétriques prédominant dans les parties moyennes et supérieures respectant souvent les apex et les culs de sacs costo-diaphragmatiques.
Stade III
Phase évolutive ou kystique, les kystes pulmonaires représentent la principale anomalie. A la phase plus tardive, l’aspect est celui d’une image en rayon de miel. Des opacités linéaires ou en bande peuvent s’y associées. Un pneumothorax est rencontré dans 15 % des cas.
La TDM en haute résolution joue un rôle primordial dans l’évaluation et l’approche diagnostic de l’histicytose à cellules de Langrhans [3, 8]. Elle montre des kystes et/ou des nodules. Les lésions subissent une évolution corrélée au stade histologique commencant par des nodules centrolobulaires à contours irréguliers (qui reflètent le caractère bronchiolocentré des lésions anatomiques de l’histiocytose X) suivis par la cavitation nodulaire (nodules troués) puis l’apparition de kystes à paroi épaisse, puis sont remplacés par des kystes à paroi fine et irrégulière. Ces lésions kystiques peuvent être isolés, jointives ou confluentes dessinant ainsi des espaces aérés de forme bizarre. Les nodules sont distribués le long des branches et des bronchioles, habituellement associés aux kystes, ils mesurent typiquement 1 à 5 mm, mais peuvent être plus longues.
Les kystes pulmonaires qui prédominent dans les formes évolués ont souvent une taille < 1cm, mais lorsqu’ils sont confluentes ils peuvent dépasser 2 cm. Ils sont ronds ou ovalaires, mais au cours de l’évolution ils peuvent prendre des formes bizarres (bi- ou multiloculés).
Une augmentation de la taille des artères pulmonaires a été rapportée chez certains patients. La TDM permet d’évoquer le diagnostic et d’orienter le prélèvement- biopsie chirurgical lorsqu’elle est réalisée [1, 3, 5, 9, 10].
Le diagnostic de certitude de l’histiocytose X repose sur la biopsie chirurgicale. Le diagnostic est facilement évoqué devant un tableau clinique et paraclinique compatible. Lorsque le contexte clinique et paraclinique est non évocateur ou atypique une biopsie par vidéo thoracoscopie guidée par la TDM en haute résolution s’impose. La biopsie d’une lésion extrathoracique, osseuse par exemple, permet parfois de parvenir indirectement au diagnostic [1, 3, 9].
Dans sa forme nodulaire le diagnostic différentiel se fait avec la pneumoconiose, la tuberculose, la pneumopathie d’hypersensibilité, les métastases et surtout la sarcoïdose. Dans sa forme kystique le diagnostic différentiel se pose essentiellement avec la lymphangiomatose pulmonaire, l’emphysème, et les bronchectasies kystiques [8, 9].
CONFLICT D’INTERETS
Aucun
REFERENCES
1. Tazi. A. Adult pulmonary Langerhans’ cell histiocytosis. Eur Respir J 2006; 27: 1272–85.
2. Konno S and Al. Adult Langerhans Cell Histiocytosis with Independently Relapsing Lung and Liver Lesions That was Successfully Treated with Etoposide. Internal medicine 2007.46.6433.
3. Nguyen K, Tazi A. Histiocytose langrahsienne de l’adulte. Revue de praticien Encyclopédie Orphanet. Novembre 2006.
4. Kim C.K and al. Pulmonary Langerhans' cell histiocytosis presented with recurrent pneumothorax. Interactive CardioVascular and Thoracic Surgery 2006; 5: 512–3.
5. Tazi A. Histiocytose langerhansienne pulmonaire de l’adulte. Encyclopédie Médico-Chirurgicale Pneumologie 2004 ; 6-039-K-30.
6. Sundar K M., Gosselin M V, Chung H L, and Cahill BC. Pulmonary Langerhans Cell Histiocytosis. Emerging Concepts in Pathobiology, Radiology, and Clinical Evolution of Disease. CHEST 2003; 123:1673–83.
7. Fournier C. et coll. Histiocytose X pulmonaire et hypothalamo-hypophysaire, diagnostiquée par biopsie cérébrale stéréotaxique. Rev Mal Respir 2004 ; 21:141-5.
8. Leatherwood D L, Heitkamp D E, Emerson R E. Pulmonary Langerhans Cell Histiocytosis. RadioGraphics 2007; 27 (1): 265-8.
9. Philippe Grenier. Imagerie thoracique de l’adulte. Flammarion Médecine-Sciences 2006.
10. Grosse C, Bankier A.A, Remmelink M, Gevenois P.A. Diagnostic des hyperclartés et des images kystiques pulmonaires de l’adulte. Encyclopédie MédicoChirurgicale Pneumologie Elsevier Masson 2007 ; 6090-C-50.
FIGURE
REFERENCES
1. Tazi. A. Adult pulmonary Langerhans’ cell histiocytosis. Eur Respir J 2006; 27: 1272–85.
2. Konno S and Al. Adult Langerhans Cell Histiocytosis with Independently Relapsing Lung and Liver Lesions That was Successfully Treated with Etoposide. Internal medicine 2007.46.6433.
3. Nguyen K, Tazi A. Histiocytose langrahsienne de l’adulte. Revue de praticien Encyclopédie Orphanet. Novembre 2006.
4. Kim C.K and al. Pulmonary Langerhans' cell histiocytosis presented with recurrent pneumothorax. Interactive CardioVascular and Thoracic Surgery 2006; 5: 512–3.
5. Tazi A. Histiocytose langerhansienne pulmonaire de l’adulte. Encyclopédie Médico-Chirurgicale Pneumologie 2004 ; 6-039-K-30.
6. Sundar K M., Gosselin M V, Chung H L, and Cahill BC. Pulmonary Langerhans Cell Histiocytosis. Emerging Concepts in Pathobiology, Radiology, and Clinical Evolution of Disease. CHEST 2003; 123:1673–83.
7. Fournier C. et coll. Histiocytose X pulmonaire et hypothalamo-hypophysaire, diagnostiquée par biopsie cérébrale stéréotaxique. Rev Mal Respir 2004 ; 21:141-5.
8. Leatherwood D L, Heitkamp D E, Emerson R E. Pulmonary Langerhans Cell Histiocytosis. RadioGraphics 2007; 27 (1): 265-8.
9. Philippe Grenier. Imagerie thoracique de l’adulte. Flammarion Médecine-Sciences 2006.
10. Grosse C, Bankier A.A, Remmelink M, Gevenois P.A. Diagnostic des hyperclartés et des images kystiques pulmonaires de l’adulte. Encyclopédie MédicoChirurgicale Pneumologie Elsevier Masson 2007 ; 6090-C-50.
ARTICLE INFO
DOI: 10.12699/jfvp.2.3.2011.37
Conflict of Interest
Non
Date of manuscript receiving
12/11/2010
Date of publication after correction
15/3/2011
Article citation
Sqalli Houssaini A, Nassar I, Malajati H, Hammani L, Ajana A, Imani F. Histiocytosis X in young smoker. J Func Vent Pulm 2011;02(05):37-39.