
 English
English
 French
French
Emergency management of penetrating chest trauma
Gestion initiale des plaies thoraciques pénétrantes aux urgences
S.Rabiou1, Y. Hama2,6, J.Didier2,6, R. Sani2,6, S. Sanoussi4,6, J. Ghalimi1, M.El Kouache3,5,7, Y. Ouadnouni1,7, M. Smahi1,7
1: Service de Chirurgie Thoracique C1, CHU Hassan II, Fès, Maroc
2: Service de Chirurgie Générale, HNN, Niamey, Niger
3: Chirurgie Cardiovasculaire, CHU Hassan II, Fès, Maroc
4: Service de Neurochirurgie, HNN, Niamey, Niger
5: Laboratoire d’Anatomie et de Chirurgie Expérimentale. Maroc
6: Faculté des Sciences de la Santé, Université Abdou Moumouni, Niamey, Niger, Maroc
7:Faculté de médecine et de pharmacie, Université Sidi Mohamed Ben Abdallah, Fès, Maroc
Corresponding author
Dr. RABIOU Sani
Service de Chirurgie Thoracique
CHU Hassan II de Fes. Maroc
E-mail: rabiousani2@icloud.com
ABSTRACT
Chest wounds are a particular entity in severe trauma as for the rest of traumatology. Indeed, the consequences of respiratory dysfunction that accompanies these wounds may be life-threatening or aggravate associated injuries. The speed of installation of hypoxemia as inflammatory processes justifies a quick answer with the adoption of comprehensive therapeutic strategies combining a severity assessment, tailored guidance, supportive care (oxygen therapy, analgesia) and etiological. If the literature on the chest wound is large in number, it seems that is very inhomogeneous in quality with many studies suffer from methodological weaknesses. The complexity of this support and no recommendation on the matter, justify the interest of our work.
KEYWORDS: Chest trauma, penetrating injury, pneumothorax, cardiac wound, emergency
RÉSUMÉ
Les plaies thoraciques représentent une entité particulière au sein de la traumatologie sévère comme pour le reste de la traumatologie. En effet, les conséquences de la dysfonction respiratoire qui accompagne ces plaies sont susceptibles d’engager le pronostic vital et/ou d’aggraver des lésions associées. La rapidité de l’installation de l’hypoxémie comme des processus inflammatoires justifie une réponse rapide avec l’adoption de stratégies thérapeutiques complètes associant une évaluation de la gravité, une orientation adaptée, une prise en charge symptomatique (oxygénothérapie, analgésie) et étiologique. Si la littérature portant sur les plaies thoraciques est importante en nombre, il s’avère qu’elle reste très inhomogène en qualité avec de nombreux travaux souffrant de faiblesses méthodologiques. La complexité de cette prise en charge et l’absence de recommandation en la matière, justifient l’intérêt de notre travail.
MOTS CLÉS: Traumatisme thoracique, plaie pénétrante, hémothorax, pneumothorax, plaie cardiaque, urgence.
INTRODUCTION
Les traumatismes thoraciques pénétrants restent toujours d’actualité dont la fréquence augmente de plus en plus a travers le monde en général et dans nos régions en particulier notamment au Maroc. L’extension de plus en plus de la violence sociale chez les jeunes, notamment liée aux difficultés socio-économiques semble expliquer cette fréquence croissante [1].
L’étiologie reste dominée dans notre contexte par les plaies par armes blanches qui constituent un véritable fléau national en rapport avec l’augmentation du taux de criminalité. Il peut aussi s’agir de poignards, de grands couteaux de cuisine, ou encore de sabres [2]. Quant aux plaies par armes à feu, elle sont très rares et souvent limitées aux accidents de chasse. Devant les exigences et les contraintes d’une meilleure prise en charge des patients victimes de plaies thoraciques, le praticien se trouve confronté à un certain nombre d’inconnues auxquelles il doit répondre précisément:
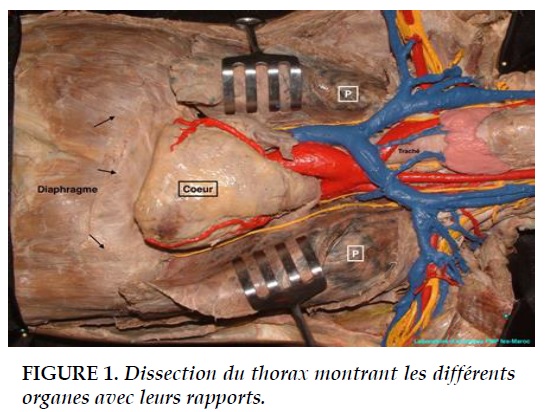
ÉLÉMENTS D’ANATOMIE THORACIQUE (FIGURE 1 )
Sur le plan anatomique, le thorax peut être séparé en 2 entités.
Un contenu mixte où siège des organes nobles
Respiratoire: l’arbre trachéo-bronchique, les plèvres et les poumons. Cardiovasculaire: le cœur, le péricarde et les gros vaisseaux du médiastin.
Un conduit digestif: œsophage.
Un conduit lymphatique: le canal thoracique qui draine surtout la lymphe sous-diaphragmatique et l’hémithorax gauche. Des nerfs appartenant au système nerveux autonome; notamment les nerfs vagues et phréniques.
Un contenant qui est constitué
D’une partie rigide: le rachis dorsal, le gril costal et le sternum, recouverts par une enveloppe musculo-aponévrotique et cutané. Une limite inférieure variable selon le moment du cycle respiratoire: il s’agit du diaphragme qui, en fonction de sa position lors d’une plaie thoracique, peut exposer des organes digestifs en plus du contenu pleural et médiastinal.
PHYSIOPATHOLOGIE
À l’état physiologique, la contraction diaphragmatique entraîne une dépression endothoracique transmise au parenchyme pulmonaire par l’existence d’un vide pleural et permettant l’expansion pulmonaire. Le sang du cœur droit ainsi oxygéné repart vers le cœur gauche et est distribué aux différents organes par la vascularisation systémique permettant l’oxygénation tissulaire.
En cas de traumatisme thoracique, il existe initialement une double défaillance respiratoire et hémodynamique dont la genèse est multifactorielle [3].
La détresse respiratoire
Elle résulte d’une atteinte de la mécanique ventilatoire et/ou d’une inadéquation ventilation/perfusion. L’atteinte des muscles de la paroi thoracique du gril costal et/ou du diaphragme altère la mécanique ventilatoire entraînant une hypoventilation alvéolaire. Ce phénomène est aggravé en cas de perte du vide pleural par la constitution d’un épanchement aérique ou liquidien qui désolidarise le poumon de la paroi thoracique et du diaphragme dont les mouvements ne lui sont plus transmis.
Le collapsus pulmonaire, lui-même causé par un pneumothorax, un hémothorax ou la compression du poumon par des organes digestifs herniés au travers d’une brèche diaphragmatique, entraîne un effet shunt (perfusion d’une partie non ventilée du poumon) qui aggrave l’hypoxémie. Cet effet shunt peut aussi être la conséquence d’une contusion pulmonaire (hématome intrapulmonaire diffusant dans les espaces interstitiels) et de l’œdème péricontusionnel, d’une inondation alvéolaire liée à une hémoptysie abondante ou de la présence de caillots dans l’arbre bronchique à l’origine d’atélectasies.
La détresse hémodynamique
Elle est liée à la présence d’un choc hémorragique et/ou cardiogénique. L’hémorragie peut être due aux plaies du cœur et des gros vaisseaux mais ces dernières conduisent rapidement à une exsanguination le plus souvent létale avant la prise en charge hospitalière. En règle générale, le choc hémorragique est le plus souvent en rapport avec la sommation d’hémorragies de moyenne abondance: une plaie d’une ou plusieurs artères pariétales (artère intercostale ou mammaire interne), plaie périphérique du parenchyme pulmonaire, système azygos. Enfin, des pertes hémorragiques extrathoraciques peuvent être associées.
Le choc hémorragique peut évoluer pour son propre compte, aboutissant à une hypothermie, une acidose et des troubles de la coagulation. Il faudra donc éviter à tout prix l’installation de cette triade létale de Moore qui rend illusoire toute possibilité d’hémostase [4].
Un choc cardiogénique peut être lié à une lésion direct du cœur, d’un pédicule coronaire, ou à la luxation du cœur au travers d’une large brèche péricardique. Il peut aussi être en rapport avec une tamponnade péricardique, particulièrement lorsque la plaie cardio-péricardique est punctiforme, ne permettant pas l’évacuation du sang dans la plèvre. Il en résulte une compression des cavités cardiaques lors de la diastole, limitant ainsi le débit cardiaque par diminution de la précharge. Initialement, ce mécanisme est compensé par une vasoconstriction périphérique et une augmentation de la fréquence et de la contractilité cardiaque. Cette compensation peut être brutalement interrompue lors d’une induction anesthésique si la tamponnade n’a pas été reconnue préalablement.
Dans le même ordre d’idée, un pneumothorax avec fuite aérienne importante (large plaie pulmonaire ou atteinte directe trachéo-bronchique) ne pouvant s’évacuer vers l’extérieur devient un pneumothorax compressif qui aggrave le collapsus pulmonaire et gêne le retour veineux au cœur. Si ces conditions se pérennisent, le médiastin se trouve refoulé vers le côté opposé, ce qui plicature les veines caves et provoque un arrêt quasi complet du retour veineux. Ce phénomène peut aboutir au désamorçage de la pompe cardiaque et au décès du blessé.
Enfin, il faut signaler la possibilité d’embolies gazeuses systémiques diffusant dans la circulation coronaire ou cérébrale. Ces embolies sont la conséquence de fistules bronchiolo-vasculaires au sein d’une plaie pulmonaire, chez des malades ventilés en pression positive lorsque celle-ci excède 40 cmH2O.
La détresse neurologique
Elle est principalement la conséquence de troubles de la conscience liée soit à des lésions associées (traumatisme crânien) soit à l’hypoxie et l’hypo-perfusion cérébrale. Elle constitue un signe de gravité de l’atteinte respiratoire et circulatoire.
LES CIRCONSTANCES DU TRAUMATISME
En pratique civile il peut s’agir d’un traumatisme au cours: d’une violence sociale par agression, ou suite aux combats de rue; d’une tentative d’autolyse; autres circonstances comme les accidents domestiques, de travail, de la voie publique, les éclats et blast, les décharges d’un fusil de chasse, ou un coup de corne de bovidé peuvent donner lieu à une plaie thoracique.
En pratique militaire les lésions thoraciques font suite à un impact direct soit: par armes blanches, par des projectiles métalliques à grande vitesse ou par éclats, qui sont plus délabrantes et souvent mortelles.
On désigne par arme blanche une lame métallique, avec un bout pointu, toutefois, tout objet pointu et suffisamment résistant peut-être à l’origine d’une plaie thoracique. Les armes blanches ont une portée lésionnelle limitée par leur longueur. Un petit canif est théoriquement potentiellement moins dangereux que la longue lame d'un couteau à cran d'arrêt.
Trois mécanismes interviennent [5]: la piqûre: conditionne la perforation et la plaie pénétrante, et dépend essentiellement de la finesse de la pointe de l’arme; la coupure ou la taille: cet effet ne permet pas généralement à l'arme de s'enfoncer dans le thorax; l’enfoncement: une fois la peau passée la lame file toute seule déterminant sur son trajet un « tunnel lésionnel » dans lequel tous les organes rencontrés peuvent être lésés.
Ainsi les principales inconnues en matière de plaies par armes blanches reste la profondeur de pénétration et la direction du trajet vulnérant.
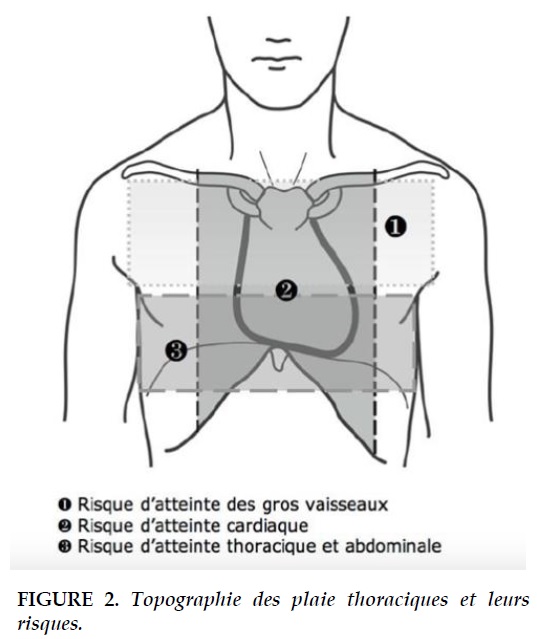
NOTION DE TOPOGRAPHIE DES PLAIES THORACIQUES (FIGURE 2)
Devant toute plaie du thorax, un examen clinique attentif est obligatoire afin de déceler les éléments nécessaires qui permettent de réaliser un diagnostic topographique des lésions:
Le siège: du ou des orifices doit être précisé par rapport aux repères anatomiques du thorax: sternum; mamelons; clavicules; lignes axillaires; bords et pointe de l’omoplate; et rebord costal. A l’issue de cet examen on peut distinguer:
La reconstitution mentale du trajet vulnérant.
La profondeur: toute plaie thoracique est considérée comme pénétrante jusqu’à preuve du contraire. La recherche d’un deuxième orifice (de sortie) qui peut être très à distance, il faut examiner avec soin le dos et le périnée, et ne pas méconnaitre un petit orifice qui peut parfois être caché dans un pli ou par du sang séché. Un seul orifice définit une plaie borgne (surtout dans les plaies par arme blanche), alors qu’un orifice d’entrée et un orifice de sortie définissent une plaie transfixiante (dans les plaies par projectile et en particulier par balle).
L’hémorragie: un saignement actif signe l’existence d’une plaie vasculaire. La paroi thoracique est richement vascularisée (pédicules musculaires, vaisseaux perforants, plaie de pédicule intercostal avec saignement extériorisé) expliquant le saignement des plaies, parfois impressionnant, pouvant entrainer à lui seule un état de choc hémorragique, en l’absence d’hémostase provisoire. Au terme de cette analyse, des examens radiologiques vont être réalisés selon l’orientation, afin de mettre en évidence les lésions pariétales et intrathoraciques possibles.
PRISE EN CHARGE INITIALE
Il est habituel de différencier 3 types de présentation.
Le blessé moribond ou en état de mort apparente
Ce cas particulier ne laisse pas de place aux examens complémentaires. Alors que les manœuvres de réanimation sont menées, une thoracotomie de sauvetage immédiate est réalisée en salle de déchocage visant à obtenir un clampage de l’aorte thoracique.
Le terme ressuscitation qualifie une thoracotomie réalisée sans délai sur un patient in extremis. Ses objectifs sont au nombre de cinq: lever une tamponnade péricardique, contrôler une hémorragie d’origine cardiaque ou vasculaire, faire l’aérostase par un clampage du hile pulmonaire, clamper l’aorte thoracique descendante et le cas échéant, réaliser un massage cardiaque interne. Les facteurs qui le plus souvent influencent la survie sont le type d’agent vulnérant (arme à feu vs arme blanche), la localisation anatomique de la lésion, enfin, la présence de signes de vie: activité électrique cardiaque, ventilation spontanée ou agonique et réponse pupillaire. Cependant, il n’y a pas d’étude prospective randomisée. Deux méta-analyses nord-américaines font référence [6,7].
La première recense 4 620 thoracotomies de ressuscitation à partir de 24 séries publiées entre 1974 et 1998. En cas de traumatisme pénétrant, la survie globale était de 8,8 % versus 1,4 % en cas de traumatisme fermé. Parmi ces traumatismes pénétrants, la survie était de 16,8 % en cas de plaie par arme blanche et de 4,3 % en cas de plaie par arme à feu. Parmi l’ensemble des blessures du tronc, celles qui étaient à prédominance cardiaque étaient associées à la survie la plus élevée 19,4 % vs 10,7 % en cas de plaie thoracique. On note également qu’en présence de signes de vie à l’admission, la survie est de 11,5 % vs 2,6 %.
La seconde méta-analyse, reprenant en partie la précédente, rapporte 4 482 thoracotomie de ressuscitation pour traumatisme pénétrant avec une survie globale de 11,2 %. La survie était de 31,1 % en cas de plaie cardiaque. Ces dernières années, plusieurs travaux ont tenté de mieux définir, outre les indications, les limites de la thoracotomie de ressuscitation. Deux séries prospectives, recensent respectivement les données de 56 et 62 patients ayant survécu après une thoracotomie de ressuscitation [8,9]. En cas de traumatisme pénétrant, cette dernière est jugée « futile » en cas de réanimation cardiopulmonaire pré-hospitalière de plus de 15 minutes avec absence de signe de vie, mais également en cas d’asystolie initiale en l’absence de tamponnade, aucun patient n’ayant survécu au-delà de ces limites.
Le blessé instable
Un blessé instable est un blessé présentant un tableau de choc hémorragique ne répondant pas aux mesures de réanimation (remplissage, vasopresseurs). C’est aussi un blessé présentant des signes qui doivent faire suspecter une tamponnade et une plaie du cœur, ces signes sont parfois complets : cyanose, tachycardie, intolérance au décubitus dorsal, triade de Beck ( turgescence des veines jugulaires, chute de la TA, assourdissement des bruits du cœur), mais souvent incomplets. Ils doivent cependant, lorsqu’ils sont associés à une plaie de l’aire cardiaque, faire considérer le blessé comme hémo-dynamiquement instable. Ces blessés doivent être conduits sans délai au bloc opératoire pour bénéficier d’un geste chirurgical.
Il est toujours souhaitable, si cela est possible, sans retarder la prise en charge, de réaliser (éventuellement au bloc pendant l’installation) une radiographie thoracique de face et une échographie recherchant un épanchement intra péritonéal associé et un épanchement péricardique. De même, il est toujours souhaitable, si l’état du blessé le permet, de drainer un hémothorax, ce qui facilite l’induction anesthésique et le temps d’exploration chirurgicale. Néanmoins, si le drain thoracique ramène un hémothorax extrêmement abondant au débit ininterrompu avec une majoration de la chute tensionnelle, il faut clamper le drain pour éviter un désamorçage cardiaque et aborder le thorax en urgence.
Plusieurs travaux ont montré que le pronostic des traumatisés les plus graves était amélioré s’ils étaient pris en charge dans des centres experts [10,11].
Cela est vérifié pour les patients qui présentent les traumatismes les plus sévères, en particulier en cas d’état de choc et/ou de coma [10-12]. Il existe un grand nombre d’études sur la prise en charge en urgence des traumatismes pénétrants du thorax. La plupart sont néanmoins rétrospectives et mono-centriques.
Dans une étude rétrospective, Mollberg s’est récemment intéressé à l’impact de la présence en salle opératoire d’un chirurgien cardio-thoracique sur la mortalité des victimes de traumatisme pénétrant du thorax [13]. Sur la période 2003–2011, 1 569 patients avaient été pris en charge dans les suites d’un traumatisme pénétrant du thorax, 413 avaient une indication chirurgicale, dont 191 (46 %) étaient décédés au cours d’une thoracotomie de ressuscitation ou avant l’arrivée au bloc.
L’analyse a été conduite sur les 222 patients opérés et sortis vivants du bloc opératoire. Les deux tiers avaient été opérés en urgence ou en extrême urgence et 35 % en urgence différée. La mortalité globale de ces patients était de 18 %. En analyse multivariée, la présence d’un chirurgien thoracique lors de la chirurgie était associée de manière indépendante à la survie. Le facteur temps est un élément crucial de la prise en charge préhospitalière des victimes de traumatisme pénétrant du thorax.
Ainsi, dans un travail rétrospectif, il a été montré, sur un collectif de 908 patients que le temps de transport préhospitalier était indépendamment associé à la mortalité des patients hypotendus à la prise en charge [14].
Le blessé stable ou stabilisé
La tomodensitométrie cervico-thoraco-abdominale permet une exploration vasculaire précise et couvre les zones charnières. Particulièrement lors d’orifices par balles, l’imagerie permet de reconstruire le trajet balistique à partir de la topographie lésionnelle et la présence de débris projectiles.
C’est la situation la plus fréquente, qui correspond à des patients qui sont soit d'emblée stable , soit après une réanimation initiale, ne présentent aucune détresse vitale. Chez ces patients, une seule question se pose: présentent-ils une lésion chirurgicale ? La prise en charge consiste donc en la réalisation d'un bilan lésionnel exhaustif, clinique et para-clinique.
La mise en condition
Elle doit être systématique, avec une position demi assise, un monitorage (TA, SpO2, ECG) et une oxygénation au besoin associée ainsi à une bonne analgésie, qui sera réalisée par paliers successifs, par voie systémique allant jusqu'à l’analgésie péridurale, si pas d’amélioration.
Evaluation clinique
L'examen clinique doit être complet de la tête aux pieds, afin de ne pas méconnaître une autre lésion pouvant engager à elle seule le pronostic vitale du patient.
Examen des fonctions vitales
Examen thoracique
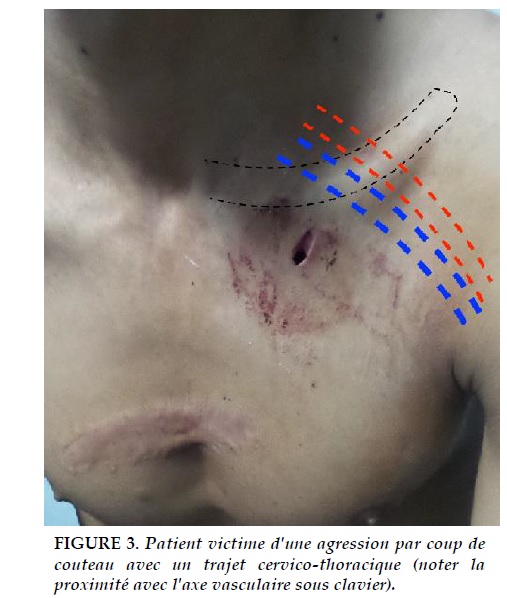
Recherche et analyse des orifices d’entrée et de sortie, avec reconstitution mentale du trajet vulnérant, recherche une plaie soufflante, un saignement, un emphysème sous cutané et son étendue, un hémi-thorax distendu immobile, un tympanisme et des anomalies à l’auscultation (Figure 3 ).
Examen abdominal
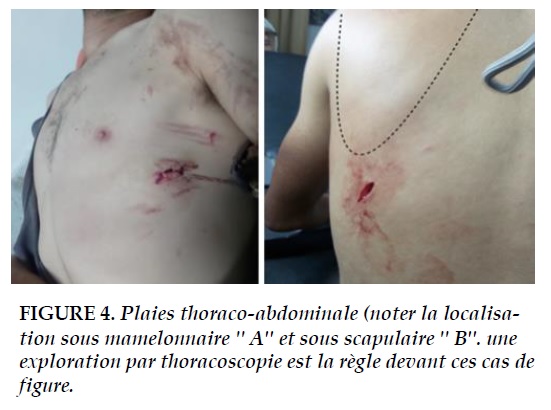
La recherche d’une plaie thoraco-abdominale ou abdominale associée dont il faut préciser le siège, une contracture ou un ventre de bois. Ainsi toute plaie en dessous de la pointe de l'omoplate en arrière ou en dessous de du mamelon en avant doit faire rechercher systématiquement une lésion diaphragmatique associée ou non à une lésion viscérale profonde et justifie la prescription urgente d'une échographie abdominale (Figure 4 A et B).
Réanimation immédiate
Une fois le bilan clinique réalisé, des mesures initiales seront instaurées en cas d’imminence d’une détresse respiratoire ou circulatoire. Cette étape a comme objectif, le rétablissement d’un état hémodynamique correct et la lutte contre toute détresse respiratoire.
Rétablissement de l’hémodynamique [15-21]
Lutte contre la détresse respiratoire
Souvent traitée par des mesures de réanimation (ponction, drainage, obturation d’un thorax soufflant, intubation orotrachéale). Seuls certains traumatismes trachéaux (plutôt cervicaux que thoraciques) ou une impossibilité d’intubation nécessitent un abord chirurgical urgent pour trachéotomie.
Rarement, l’association d’une hémoptysie abondante à un emphysème sous cutané extensif peut faire évoquer une plaie trachéo-bronchique associée à une plaie vasculaire.
Une intubation sélective par une sonde à double courant (ou par une sonde trachéale poussée en intrabronchique) peut alors être tentée pour mettre le patient à l’abri d’une inondation bronchique controlatérale à la lésion en attendant un geste chirurgical.
Restauration d’une ventilation correcte par
LES MODALITES DE L’EXPLORATION D’UNE PLAIE DE L’AIRE CARDIAQUE EN URGENCE
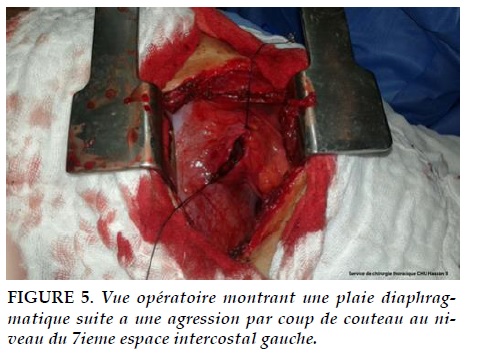
On entend par aire cardiaque la zone comprise entre les 2 clavicules et la fourchette sternale, en haut, les deux lignes médioclaviculaires, latéralement, et l’auvent costal, en bas (Figure 5).
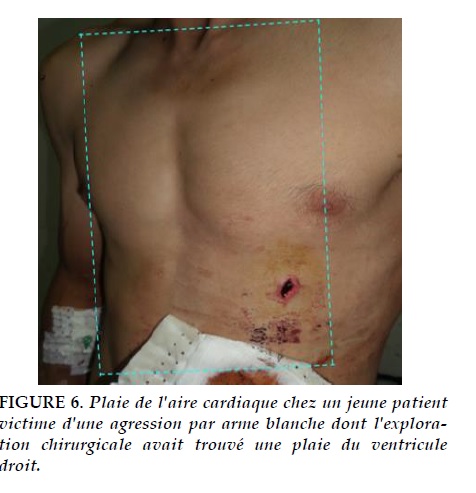
Sont incluses également les plaies transmédiastinales. Il existe un nombre important d’études sur les plaies de l’aire cardiaque (Figure 6). La majorité de ces études est rétrospective uni- ou multicentrique, parfois prospective, mais aucune, à notre connaissance, randomisée. L’échographie a maintenant supplanté la fenêtre péricardique pour le diagnostic des épanchements péricardiques post-traumatiques. Dans une série prospective de 261 patients, Rozycki et al. [23] rapportent une sensibilité de 100 %, une spécificité de 97 %, une valeur prédictive positive de 80,6 % et une valeur prédictive négative de 100 %. Récemment, Ball et al. [24], dans une étude rétrospective concernant 228 patients avec plaie cardiaque, rapportent 5 cas de faux négatifs, tous associés à un hémothorax gauche. De manière similaire, Meyer et al. [25], dans une série prospective de 105 patients, rapportent 4 cas de faux négatifs, tous présentant un épanchement pleural, avec une sensibilité de l’échographie chutant à 55,6 %. Deux mécanismes sont avancés pour expliquer ce fait: la décompression du péricarde dans la plèvre en cas de brèche importante ou la gêne liée à l’hémothorax, empêchant la bonne visualisation du sac péricardique. En l’absence d’hémothorax, les auteurs concluent néanmoins à l’équivalence de l’échographie et de la fenêtre péricardique par voie sous-xiphoïdienne.
L’ensemble des données de la littérature plaide pour une exploration chirurgicale systématique en urgence en cas d’épanchement péricardique mais ne permet pas de proposer de recommandation quant à la voie d’abord.
Au total, les experts suggèrent l’abord chirurgical du thorax (thoracotomie antéro-latérale gauche, transverse ou sternotomie) en urgence en cas d’instabilité hémodynamique et/ou d’épanchement péricardique compressif à l’échographie. Une surveillance simple, en milieu spécialisé, en l’absence d’épanchement péricardique, d’hémothorax et de stabilité hémodynamique stricte après bilan tomodensitométrique.
CONCLUSION
La prise en charge des plaies thoraciques nécessite une organisation logistique et matérielle préalable. L’ensemble des acteurs (urgentiste, chirurgien, anesthésiste-réanimateur, radiologue, et biologiste) doivent s’entendre sur des protocoles de prise en charge tenant compte à la fois des moyens disponibles en pratique, de leurs délais de mise en œuvre et du rôle de chacun dans la chaine de la prise en charge qui doit être rapide et adaptée.
CONFLIT D’INTÉRÊT
Pas de lien d’intérêt avec cet article.
RÉFÉRENCES
1. Ouadnouni Y, Ghalimi J, Lakranbi M, Smahi M. Les plaies thoraciques. Journal Marocain des Sciences Médicales 2014;19(2):1-12.
2. Housni B, Khatouf M, Harandou M, Kanjaa N. Prise en charge des plaies thoraciques par arme blanche au service de réanimation chirurgicale de Fès. J Magh A Réa 2004; 9: 215-16.
3. Avaro JP, D’journo X B, Trousse D, Roch A, Thomas P A, Doddoli C. Le traumatisme thoracique grave aux urgences, stratégie de prise en charge initiale Reanimation, 15 (2006), pp. 561–567.
4. Moore FA, McKinley BA, Moore A. The next generation in shock resuscitation Lancet 2004;363 pp.1988–96.
5. Cador L, Lonjon T. Plaies thoraciques. EMC, Urgences 1997. 24–103–A10;9p.
6. Rhee PM, Acosta J, Bridgeman A, Wang D, Jordan M, Rich N. Survival after emergency department thoracotomy: review of published data from the past 25 years. J Am Coll Surg 2000;190:288–298.
7. Working Group, Ad Hoc Subcommittee on Outcomes, American College of Surgeons–Committee on Trauma Practice Management Guidelines for Emergency Department Thoracotomy. J Am Coll Surg 2001;1993:303–309.
8. Moore EE, Knudson M.M. , Burlew C.C, Inaba K., Dicker R.A., Biffl W.L. , et al. Defining the limits of resuscitative emergency department thoracotomy: a contemporary Western Trauma Association perspective. J Trauma 2011;70:334–339.
9. Powell D.W, Moore E.E. , Cothren C.C., Ciesla D.J., Burch J.M., Moore J.B. , et al. Is emergency department resuscitative thoracotomy futile care for the critically injured patient requiring prehospital cardiopulmonary resuscitation? J Am Coll Surg 2004;199:211–215
9. Nathens A.B., Jurkovich G.J., Maier R.V., Grossman D.C., MacKenzie E.J., Moore M. , et al. Relationship between trauma center volume and outcomes JAMA 2001;285:1164–1171.
10. MacKenzie E.J., F.P. Rivara, G.J. Jurkovich, et al. A national evaluation of the effect of trauma-center care on mortality N Engl J Med, 354 (2006), 366–378.
11. Demetriades D., M. Martin, A. Salim, P. Rhee, C. Brown, J. Doucet, et al. Relationship between American College of Surgeons trauma center designation and mortality in patients with severe trauma (injury severity score > 15). J Am Coll Surg, 202 (2006),212–215.
12. N.M. Mollberg, D. Tabachnik, F. Farjah, F.-J. Lin, A. Vafa, K. Abdelhady, et al. Utilization of Cardiothoracic Surgeons for Operative Penetrating Thoracic Trauma and Its Impact on Clinical Outcomes Ann Thorac Surg 2013;96:445–450.
13. M. Swaroop, D.C. Straus, O. Agubuzu, T.J. Esposito, C.R. Schermer, M.L. Crandall Pre-hospital transport times and survival for hypotensive patients with penetrating thoracic trauma. J Emerg Trauma Shock 2013;6:16–20.
14. Riou B. Prise en charge à l’hôpital des traumatismes du thorax. In : Traumatologie thoracique aiguë. Société d’imagerie thoracique. Journal de radiologie 1997; 820 33.
15. Jancovici R, Diraison Y, Pons F, Jeanbourquin D, Brinquin L, Dumurgier C. Chirurgie d'hémostase des plaies et traumatismes du thorax. In: Le choc hémorragique. Collection d'Anesthesiologie et de Réanimation. Paris: Masson,1991.Chapitre II, 125-151.
16. Riou B, Goarin JP. Traumatismes thoraciques. In : Samii K. Anesthésie- Réanimation chirurgical 2ème édition. 1995;161:P:1606-14.
17. Télion C, Carli P. Etats de choc et remplissage. In : SFAR Médecine d’urgence 2001;P: 39-48.
18. Plaisance P, Ducos L. Prise en charge des états de choc : Démarche préhospitalière. SFAR Médecine d’urgence 2001;P:17-25.
19. Gérard J L, Pondaven E, Lehaux P, Bricard H. Transfusion, autotransfusion en urgence. In: SFAR Médecine d’urgence 2001;P:95-102.
20. Gueugnicaud P Y, Macabeo C, Ruiz ., Zeghari M. Catécholamines dans les états de choc. In: SFAR Médecine d’urgence 2001;P:49-60.
21. Barone JE et al. Indications for intubation in blunt chest trauma. J. Trauma. 1986; 26; p:334-8.
22. G.S. Rozycki, D.V. Feliciano, M.G. Ochsner, M.M. Knudson, D.B. Hoyt, F. Davis, et al. The role of ultrasound with possible penetrating cardiac wounds: a prospective multicenter study J Trauma 1999;46:543–551.
23. C.G. Ball, B.H. Williams, A.D. Wyrzykowski, J.M. Nicholas, G.S. Rozycki, D.V. Feliciano A caveat to the performance of pericardial ultrasound in patients with penetrating cardiac wounds J Trauma 2009;67:1123–1124.
24. D.M. Meyer, M.E. Jessen, P.A. Grayburn Use of echocardiography to detect occult cardiac injury after penetrating trauma: a prospective study. J Trauma 1995;39: 902.
FIGURES AND TABLE

REFERENCES
1. Ouadnouni Y, Ghalimi J, Lakranbi M, Smahi M. Les plaies thoraciques. Journal Marocain des Sciences Médicales 2014;19(2):1-12.
2. Housni B, Khatouf M, Harandou M, Kanjaa N. Prise en charge des plaies thoraciques par arme blanche au service de réanimation chirurgicale de Fès. J Magh A Réa 2004; 9: 215-16.
3. Avaro JP, D’journo X B, Trousse D, Roch A, Thomas P A, Doddoli C. Le traumatisme thoracique grave aux urgences, stratégie de prise en charge initiale Reanimation, 15 (2006), pp. 561–567.
4. Moore FA, McKinley BA, Moore A. The next generation in shock resuscitation Lancet 2004;363 pp.1988–96.
5. Cador L, Lonjon T. Plaies thoraciques. EMC, Urgences 1997. 24–103–A10;9p.
6. Rhee PM, Acosta J, Bridgeman A, Wang D, Jordan M, Rich N. Survival after emergency department thoracotomy: review of published data from the past 25 years. J Am Coll Surg 2000;190:288–298.
7. Working Group, Ad Hoc Subcommittee on Outcomes, American College of Surgeons–Committee on Trauma Practice Management Guidelines for Emergency Department Thoracotomy. J Am Coll Surg 2001;1993:303–309.
8. Moore EE, Knudson M.M. , Burlew C.C, Inaba K., Dicker R.A., Biffl W.L. , et al. Defining the limits of resuscitative emergency department thoracotomy: a contemporary Western Trauma Association perspective. J Trauma 2011;70:334–339.
9. Powell D.W, Moore E.E. , Cothren C.C., Ciesla D.J., Burch J.M., Moore J.B. , et al. Is emergency department resuscitative thoracotomy futile care for the critically injured patient requiring prehospital cardiopulmonary resuscitation? J Am Coll Surg 2004;199:211–215
9. Nathens A.B., Jurkovich G.J., Maier R.V., Grossman D.C., MacKenzie E.J., Moore M. , et al. Relationship between trauma center volume and outcomes JAMA 2001;285:1164–1171.
10. MacKenzie E.J., F.P. Rivara, G.J. Jurkovich, et al. A national evaluation of the effect of trauma-center care on mortality N Engl J Med, 354 (2006), 366–378.
11. Demetriades D., M. Martin, A. Salim, P. Rhee, C. Brown, J. Doucet, et al. Relationship between American College of Surgeons trauma center designation and mortality in patients with severe trauma (injury severity score > 15). J Am Coll Surg, 202 (2006),212–215.
12. N.M. Mollberg, D. Tabachnik, F. Farjah, F.-J. Lin, A. Vafa, K. Abdelhady, et al. Utilization of Cardiothoracic Surgeons for Operative Penetrating Thoracic Trauma and Its Impact on Clinical Outcomes Ann Thorac Surg 2013;96:445–450.
13. M. Swaroop, D.C. Straus, O. Agubuzu, T.J. Esposito, C.R. Schermer, M.L. Crandall Pre-hospital transport times and survival for hypotensive patients with penetrating thoracic trauma. J Emerg Trauma Shock 2013;6:16–20.
14. Riou B. Prise en charge à l’hôpital des traumatismes du thorax. In : Traumatologie thoracique aiguë. Société d’imagerie thoracique. Journal de radiologie 1997; 820 33.
15. Jancovici R, Diraison Y, Pons F, Jeanbourquin D, Brinquin L, Dumurgier C. Chirurgie d'hémostase des plaies et traumatismes du thorax. In: Le choc hémorragique. Collection d'Anesthesiologie et de Réanimation. Paris: Masson,1991.Chapitre II, 125-151.
16. Riou B, Goarin JP. Traumatismes thoraciques. In : Samii K. Anesthésie- Réanimation chirurgical 2ème édition. 1995;161:P:1606-14.
17. Télion C, Carli P. Etats de choc et remplissage. In : SFAR Médecine d’urgence 2001;P: 39-48.
18. Plaisance P, Ducos L. Prise en charge des états de choc : Démarche préhospitalière. SFAR Médecine d’urgence 2001;P:17-25.
19. Gérard J L, Pondaven E, Lehaux P, Bricard H. Transfusion, autotransfusion en urgence. In: SFAR Médecine d’urgence 2001;P:95-102.
20. Gueugnicaud P Y, Macabeo C, Ruiz ., Zeghari M. Catécholamines dans les états de choc. In: SFAR Médecine d’urgence 2001;P:49-60.
21. Barone JE et al. Indications for intubation in blunt chest trauma. J. Trauma. 1986; 26; p:334-8.
22. G.S. Rozycki, D.V. Feliciano, M.G. Ochsner, M.M. Knudson, D.B. Hoyt, F. Davis, et al. The role of ultrasound with possible penetrating cardiac wounds: a prospective multicenter study J Trauma 1999;46:543–551.
23. C.G. Ball, B.H. Williams, A.D. Wyrzykowski, J.M. Nicholas, G.S. Rozycki, D.V. Feliciano A caveat to the performance of pericardial ultrasound in patients with penetrating cardiac wounds J Trauma 2009;67:1123–1124.
24. D.M. Meyer, M.E. Jessen, P.A. Grayburn Use of echocardiography to detect occult cardiac injury after penetrating trauma: a prospective study. J Trauma 1995;39: 902.
ARTICLE INFO
DOI: 10.12699/jfvp.7.20.2016.6
Conflict of Interest
Non
Date of manuscript receiving
25/4/2015
Date of publication after correction
10/3/2016
Article citation
Rabiou S, Hama Y, Didier J, Sani R, Sanoussi S, Ghalimi J, Kouache M.El, Ouadnouni Y, Smahi M. Emergency management of penetrating chest trauma. J Func Vent Pulm 2016;20(7):6-14.