
 English
English
 French
French
Traitement du syndrome d’apnées du sommeil par pression positive nocturne
Treatment of sleep apnea syndrome by positive pressure at night
D. Baud
Centre Hospitalier Spécialisé en Pneumologie
94669 Chevilly Larue - France
Corresponding author
Dr. Dany BAUD
Centre Hospitalier Spécialisé en Pneumologie. 24 rue Albert Thuret, 94669 Chevilly Larue - France
E-mail: danybaud@chsp.asso.fr
ABSTRACT
Sleep apnea syndrome in its obstructive form (OSAS) is a disease that has been known since the late fifties. It is characterized by snoring often high intensity interrupted by pauses of breathing or simple decreases of breathing amplitude due to total or partial collapse of the hypopharynx.
The reflex restoration of normal respiratory flow can make only awakenings with respiratory efforts resulting relief and fragmentation of sleep. It is responsible for the main daytime symptom with excessive sleepiness. Logical treatment of this pathological cascade is to keep opening of upper airway during sleep. Since 1981 , the date of publication of Sullivan et al. in treatment of OSAS by continuous positive airway pressure (CPAP), this therapy has become the standard in moderate to severe symptomatic forms of this disease.
The effectiveness of this treatment on the main symptom with sleepiness of this disease is indisputable. Although significant technical progress (noise, dimension, quality of interfaces) has been made, the tolerance of this instrumental treatment poses no less real problem in a significant number of patients.
KEYWORDS: OSAS, snoring, sleepiness, CPAP
RÉSUMÉ
Le syndrome d’apnées du sommeil dans sa forme obstructive (SAOS) est une maladie connue depuis la fin des années cinquante. Il se caractérise par un ronflement souvent de forte intensité interrompu par des pauses respiratoires ou de simples diminutions d’amplitude de la respiration par collapsus total ou partiel de l’hypopharynx.
Le rétablissement réflexe d’un flux respiratoire normal ne peut se faire qu’au prix d’éveils avec efforts respiratoires entraînant un allégement et une fragmentation du sommeil responsable du symptôme diurne principal qui est la somnolence excessive. Le traitement logique de cette cascade pathologique est de maintenir ouvertes les voies aériennes supérieures pendant le sommeil. Depuis 1981, date de la publication de Sullivan et coll. sur le traitement du SAOS par pression positive continue (PPC), cette thérapeutique est devenue la référence dans les formes symptomatiques modérées à sévères de cette affection.
L’efficacité de cette thérapeutique sur la somnolence symptôme principal de cette maladie est incontestable. Même si des progrès techniques notables (bruit, encombrement, qualité des interfaces) ont été accomplis, la tolérance de ce traitement instrumental pose un problème non moins réel chez un nombre important de patients.
MOTS CLES: SAOS, ronflement, somnolence, PPC
INTRODUCTION
Le syndrome d’apnées du sommeil dans sa forme obstructive (SAOS) est une maladie connue depuis la fin des années cinquante. Il se caractérise par un ronflement souvent de forte intensité interrompu par des pauses respiratoires ou de simples diminutions d’amplitude de la respiration par collapsus total ou partiel de l’hypopharynx. Le rétablissement réflexe d’un flux respiratoire normal ne peut se faire qu’au prix d’éveils avec efforts respiratoires entraînant un allégement et une fragmentation du sommeil responsable du symptôme diurne principal qui est la somnolence excessive. Les autres conséquences nocturnes des anomalies respiratoires et des éveils sont l’hypoxémie et l’activation du système sympathique. Elles expliquent pour une part l’excès de maladies cardiovasculaires des patients atteints de SAOS.
Le traitement logique de cette cascade pathologique est de maintenir ouvertes les voies aériennes supérieures pendant le sommeil. Depuis 1981, date de la publication de Sullivan et coll. sur le traitement du SAOS par pression positive continue (PPC), cette thérapeutique est devenue la référence dans les formes symptomatiques modérées à sévères de cette affection [1, 2].
DESCRIPTION
Le dispositif de PPC est constitué d’un générateur de pression relié par l’intermédiaire d’un tuyau à un masque nasal ou facial fixé sur le visage du patient à l’aide d’un harnais. Son emploi nécessite une alimentation électrique. L’air propulsé peut être humidifié par un dispositif séparé ou intégré.
LE MECANISME D’ACTION DE LA PPC
La PPC agit à la manière d’une attelle pneumatique. Utilisée au cours du sommeil, elle s’oppose au collapsus pharyngé en délivrant dans les voies aériennes supérieures de l’air à une pression faiblement supérieure à la pression atmosphérique, généralement voisine de 10 cm d’eau. Les différentes imageries ont montré que la pression positive augmente le diamètre des voies aériennes supérieures tant chez les sujets éveillés qu’endormis.
Elle accroît également le volume pulmonaire avec pour conséquence possible la traction de la trachée vers le bas qui à son tour mettrait en tension les voies aériennes supérieures et augmenterait leur calibre. La pression requise au maintien de l’ ouverture des voies aériennes supérieures pendant le sommeil dépend de leur tendance particulière au collapsus, laquelle est augmentée en position allongée, au cours du sommeil paradoxal, en cas de prise de poids et lors de la consommation d’alcool et de sédatif [3].
LES MODES DE PRESSION POSITIVE
Historiquement, le mode constant c'est-à-dire en pression fixe a été le premier et le plus largement utilisé. Dans la perspective d’une meilleure tolérance ou au cours de situations particulières, d’autres modes ont été conçus: à double niveau de pression, à pression pilotée ou auto ajustée, à pression expiratoire flexible et la ventilation auto asservie. Dans tous les cas, la pression positive ne peut être inférieure à une valeur minimale (3 à 4 cm d’eau) permettant la circulation de l’air dans le circuit et s’opposant ainsi au phénomène de ré inhalation du CO2 expiré (rebreathing).
Mode constant Une même pression fixe est délivrée au cours de l’inspiration et l’expiration du patient. Le niveau de pression nécessaire à la disparition des événements respiratoires anormaux (apnées et hypopnées) est défini par titration. Initialement et de façon idéale, celle-ci était effectuée manuellement en laboratoire de sommeil. Au cours d’un enregistrement polysomnographique nocturne, un technicien, par montées progressives de la pression, détermine celle requise à la normalisation du tracé. Cette technique coûteuse en homme, en temps et en matériel a été progressivement remplacée par l’auto-titration. Le niveau de pression efficace retenu est celui permettant de corriger 90 à 95% des événements respiratoires au cours d’une nuit de traitement par PPC autopilotée. Cette titration peut se faire au domicile du patient [4].
Mode a double niveau de pression
Le générateur délivre de façon séparée et ajustée une pression expiratoire basse et une pression inspiratoire haute (EPAP et IPAP des auteurs anglo-saxons). Initialement utilisée chez les sujets tolérant mal d’ expirer contre une pression trop élevée, elle est actuellement réservée aux patients atteints de maladies respiratoires associées au SAOS (overlap syndrome, syndrome d’obésité et hypoventilation) dans le cas où la PPC seule ne suffit pas à corriger les échanges gazeux [5].
Mode a pression pilotée ou auto ajustée
Les PPC autopilotées (APAP) choisissent de façon automatique, dans un intervalle prédéterminé, les niveaux de pression selon la survenue et l’intensité des événements respiratoires. Cette intervention « à la demande » permet finalement au cours de la nuit d’utiliser une pression moyenne efficace moins élevée que celle d’un mode constant [6].
L’intérêt essentiel et théorique du mode auto ajusté est d’améliorer la tolérance de la PPC chez certains patients. Elle permet aussi de s’affranchir du temps de la titration. Ce mode, comme on l’a vu plus haut, est également employé lors de la titration pour le mode constant.
Mode a pression expiratoire flexible
Il s’agit davantage d’une option que d’un mode à part entière, d’ailleurs applicable à tous les modes sus cités. Elle permet la baisse modérée de la pression (1 à 3 cm d’eau) au début de l’expiration, suivie d’un retour à la pression efficace en fin d’expiration [7].
Ventilation auto asservie
Elle est assurée par un appareil de pression positive récemment développé pour le traitement des syndromes d’apnées du sommeil centraux, notamment de la respiration de Cheyne-Stockes de l’insuffisance cardiaque. Ce mode de ventilation peut être aussi appliqué en cas de syndromes d’apnées dits complexes associant apnées obstructives et centrales. Son principe consiste à adapter la différence entre la pression expiratoire assurant l’ouverture des voies aériennes supérieures et la pression inspiratoire de façon à stabiliser la ventilation du patient en la maintenant aux environs de 90% de sa valeur moyenne lors de la survenue d’hypo ou d’hyperventilation ainsi qu’au cours d’apnées centrales qui sont par conséquent corrigées [8].
HUMIDIFICATION ET INTERFACES
Humidification
L’air froid délivré par les PPC peut chez certains patients provoquer au niveau des muqueuses du nez et de la bouche une sécheresse ou une congestion augmentant les résistances nasales, notamment en cas de fuite et particulièrement lors des phénomènes d’ouverture buccale. La plupart des dispositifs de pression positive sont équipés d’humidificateurs chauffants qui pallient le plus souvent ces effets secondaires.
Les interfaces
Ce terme désigne les différents masques utilisables qu’il s’agisse de masque nasal ou facial, d’embouts narinaires ou plus rarement de dispositif endobuccal. Le masque nasal et le masque facial sont le plus souvent utilisés. Ils sont en silicone, disponibles en plusieurs tailles et possèdent un orifice de fuite qui permet au gaz carbonique de s’évacuer. Comme nous le verrons plus loin dans le chapitre consacré aux effets secondaires et à la tolérance de la PPC, même si des progrès considérables ont été faits en termes de possibilités de choix, c’est le plus souvent des problèmes d’interface qui sont à l’origine de l’interruption du traitement.
INDICATIONS ET EFFETS BENEFIQUES DU TRAITEMENT PAR PPC
Indications
Le traitement par PPC est le traitement de référence du SAOS dans sa forme modérée à sévère, c'est-àdire dont l’index d’événements respiratoires est supérieur ou égal à 15/heure.
En France, la prise en charge de ce traitement par l’Assurance Maladie est conditionnée à l’existence d’un index d’apnées + hypopnées (IAH) ≥ 30/heure ou d’un index de micro éveils liés aux efforts respiratoires ≥ 10/heure. Dans ces 2 cas le patient doit présenter 3 signes ou symptômes du SAOS (ronflement, somnolence, céphalée, nycturie, HTA...). Aux EtatsUnis, un IAH ≥ 15/heure avec ou sans symptômes suffit au remboursement. En cas d’IAH ≥ 5/heure et < 15, l’existence de symptômes est alors nécessaire.
Effets bénéfiques du traitement par PPC
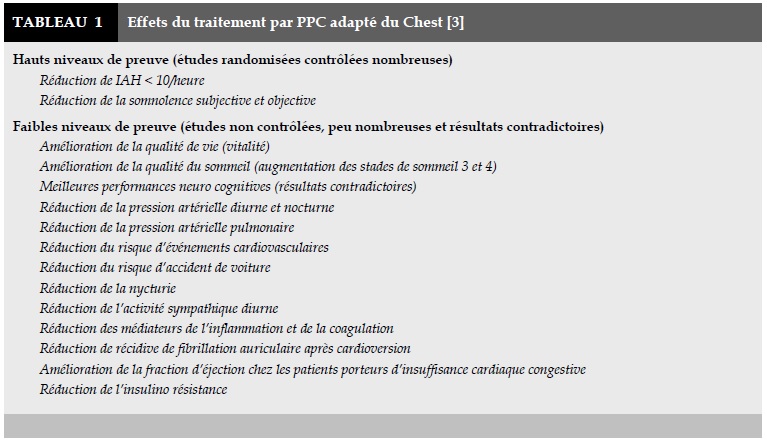
De multiples études, dont certaines ont fait l’objet en 2003 et 2006 de synthèses méthodiques du Réseau Cochrane, permettent d’évaluer les effets bénéfiques du traitement par PPC au cours du SAOS (Tableau 1). L’amélioration porte sur les symptômes notamment les troubles de vigilance, la qualité de vie, l’incidence des complications cardiovasculaires et la fréquence des accidents de la circulation. Comme habituellement, les niveaux de preuve de ces améliorations varient en fonction du nombre d’études, du nombre de patients concernés et de l’existence éventuelle d’un groupe placebo (PPC délivrant une pression infra thérapeutique) [9-10].
Effets indésirables
Les principaux effets indésirables décrits sont:
+ Gêne due au bruit de l’appareil (environ 30dB).
+ Lésions cutanées (irritation, blessure, escarre) dues à un contact trop appuyé du masque sur la peau du visage et en particulier sur l’arête du nez.
+ Congestion nasale et rhinorrhée liées à l’air froid et aggravées par les fuites.
+ Sécheresse des muqueuses par fuites au masque et ouverture de bouche.
+ Douleurs au contact du masque et du harnais.
+ Conjonctivite liée aux fuites.
+ Altération du sommeil.
+ Sensation de suffocation liée à la pression.
+ Claustrophobie.
+ Aérophagie.
+ Gêne pour le conjoint (bruit, courant d’air).
+ Plus rarement allergie cutanée, épistaxis, infection ORL.
Les synthèses méthodiques Cochrane ne rapportent pas d’incidences fiables de ces divers effets indésirables [9, 10].
MODALITES DE MISE EN PLACE ET DE SUIVI
Mise en place
Le traitement par PPC peut être initié soit au domicile du patient, soit en milieu hospitalier. En pratique, le choix des thérapeutes repose davantage sur leurs conditions d’exercice et les moyens dont ils disposent que sur une opinion préalable. Même si il n’existe pas d’études démontrant la supériorité d’un lieu par rapport à l’autre, il semble raisonnable de penser qu’un traitement complexe et intrusif comme la PPC nécessite pour être accepté et supporté un temps dédié suffisant et un accompagnement technique et psychologique adapté. Une mise en place au domicile effectuée par nécessité dans la journée et non pendant la période de sommeil avec un accompagnement ponctuel, donc de courte durée, ne peut répondre entièrement à ces conditions.
Le schéma suivant de mise en place en milieu hospitalier peut être proposé:
Un après midi où seront effectués
L’accueil du patient par l’équipe pluridisciplinaire.
Une éducation thérapeutique initiale (diagnostic éducatif, objectifs pédagogiques…), poursuivie ensuite à toutes les étapes de la mise en place notamment en terme d’apprentissage et d’évaluation.
Le choix des matériels (type d’appareillage, masque, harnais, éventuelle humidification…) après contrôle de la perméabilité nasale (interrogatoire, mesure du débit inspiratoire nasal de pointe) et thérapeutique correctrice si nécessaire.
L’essai et l’adaptation.
Une nuit sous surveillance et accompagnement du personnel infirmier spécialisé où seront effectué
La mise en place de l’appareillage choisi l’après midi.
La titration.
Le contrôle oxymétrique.
Au réveil où seront effectués
Un entretien-discussion avec le patient sur son ressenti de la tolérance (douleur provoquée par le masque, fuites perçues, claustrophobie…), de l’éventuelle efficacité immédiate (qualité de sommeil, nycturie, asthénie matinale, céphalées…) et sur ses capacités et son souhait de prolonger l’essai à domicile.
La récupération des données enregistrées:
+ Niveaux de pressions qui permettront de choisir entre modes piloté (détermination des limites haute et basse) ou constant.
+ Index d’apnées-hypopnées résiduel dont la valeur doit être inférieure à 10/heure.
+ Rechercher les causes et apporter une correctiRechercher les causes et apporter une correction en cas d’index plus élevé.
+ Fuites excessives éventuelles. Rechercher leurs causes (masque, harnais, ouverture de bouche…) et apporter une correction.
+ Oxymétrie corrigée. Rechercher les causes et apporter une correction en cas de désaturations notables persistantes.
Suivi
A court terme
C’est certainement au cours des premiers jours de traitement que se joue l’observance à long terme de la PPC. Une mauvaise tolérance initiale et un défaut de correction des différents problèmes techniques qui en sont la cause risquent de conduire à un arrêt précoce du traitement et à un refus ultérieur d’appareillage. En conséquence, il convient que médecin prescripteur et prestataire de service soient joignables pour que conseils, encouragements et interventions techniques correctrices puissent être proposés dans les meilleurs délais.
En pratique après un mois de traitement, le patient (idéalement accompagné de son conjoint) est revu par le médecin prescripteur avec tout son matériel (PPC et interface) et un relevé d’observance obtenu sur place ou fourni par le prestataire.
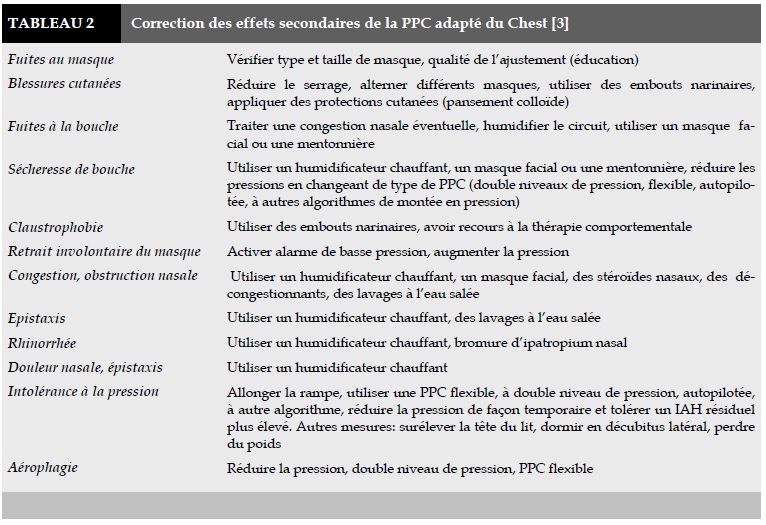
Dans un premier temps seront évalués la tolérance, les effets secondaires et les bénéfices ressentis. Seront ensuite contrôlés à partir des relevés de machine, l’observance, l’IAH résiduel, le niveau de fuite et les niveaux de pression en cas de PPC autopilotée. En cas de problèmes (Tableau 2), des corrections seront apportées dont les résultats seront évaluées lors d’une prochaine consultation programmée. Toutes ces mesures seront effectuées en collaboration étroite avec le prestataire de service.
Le bénéfice clinique du traitement par PPC, notamment la réduction de somnolence survient en une 1 à 2 semaine. Dans le cas contraire, si l’observance est satisfaisante (supérieure à 4 heures par nuit), la tolérance bonne et l’efficacité contrôlée, il conviendra d’effectuer une polysomnographique sous PPC à la recherche d’une fragmentation du sommeil par des efforts respiratoires persistants ou des mouvements périodiques des jambes. Un tracé normalisé fera rechercher à l’origine de la somnolence, une autre cause que le SAOS.
A moyen et long terme
Une fois obtenues une tolérance, une observance et une efficacité satisfaisantes, une surveillance médicale annuelle est suffisante, d’autant qu’en France elle est associée de façon réglementaire à une visite semestrielle par le prestataire (relevé d’observance, évaluation de l’efficacité et de la tolérance, contrôle technique de la PPC et des interfaces). Des consultations non programmées ont lieu dans les circonstances suivantes: défaut d’observance, baisse d’efficacité et survenue d’événement médical indésirable évoquant une complication possible d’un SAOS mal contrôlé.
•Défaut d’observance: a long terme, un défaut d’observance est rarement d’origine technique. En dehors d’une guérison du SAOS par une perte de poids significative entrainant une intolérance à la PPC, il a le plus souvent des causes psycho-sociales (changement de mode de vie, de partenaire, syndrome dépressif…) qu’il faudra identifier et prendre en charge. En cas de lassitude et de désir confirmé d’arrêt de traitement par PPC, on pourra après discussion et information proposer au patient une thérapeutique alternative, notamment l’orthèse d’avancée mandibulaire si elle s’avère possible.
• Baisse d’efficacité: après avoir éliminé une baisse d’observance, des pressions insuffisantes du fait le plus souvent d’une prise de poids, une somnolence d’une autre origine (maladie associée, prise médicamenteuse sédative…), on effectuera une polysomnographique sous PPC à la recherche d’une fragmentation du sommeil.
• Survenue d’événement médical indésirable évoquant une complication possible d’un SAOS mal contrôlé: c’est essentiellement en cas d’événement cardio-vasculaire survenant chez un patient traité par PPC qu’il faudra contrôler l’efficacité de ce traitement par polysomnographie afin de ne pas méconnaitre des efforts respiratoires persistant fragmentant le sommeil et responsables d’une hypertonie sympathique, ainsi que des désaturations nocturnes de l’oxyhémoglobine.
ACCEPTATION ET OBSERVANCE
Le traitement par pression positive du syndrome d’apnées du sommeil est un des seuls traitements de maladie chronique contrôlable et mesurable du fait des différents dispositifs électroniques intégrés à l’appareillage. Pour être efficace, la durée d’utilisation nocturne d’une PPC ne doit pas être trop inférieure à celle du sommeil spontané et si cette durée d’utilisation est trop courte le rapport bénéfice / contrainte devient rapidement défavorable.
Acceptation de la PPC
C’est accepter de faire l’essai de la PPC pendant quelques jours (» 7j) après une titration initiale. Selon les données de la littérature, le taux d’acceptation se situe aux environ de 80% [11].
Adhésion à la PPC
C’est l’observance de la PPC au moins 4 heures par nuit, 70% des nuits. Selon les données de la littérature, l’adhésion se situe autour de 70% à trois ans [12]. Ce taux d’observance est supérieur à celui de l’observance médicamenteuse au cours des maladies chroniques, lequel ne dépasse pas 60%. Généralement la qualité de l’observance des 3 premiers mois est prédictive de celle au long cours.
Les facteurs prédictifs d’adhésion à la PPC sont la sévérité du SAOS en termes de somnolence et d’index d’apnées - hypopnées et la perception du bénéfice du traitement. A l’inverse, les facteurs prédictifs négatifs sont l’absence de somnolence et de bénéfice perçu du traitement, les effets secondaires de la PPC, l’uvulo-pharyngoplastie, l’obstruction nasale et la claustrophobie.
Méthodes pour améliorer l’observance
L’observance rapportée dans les études les plus anciennes était celle déclarée par les patients. Elle se situe entre 50 et 85% du temps total de sommeil [13]. Les études actuelles concernent l’observance réelle obtenue à partir des relevés d’observance des machines et ne tiennent compte que du temps pendant lequel le masque est en place. Elles montrent que les patients surestiment leur durée d’utilisation de PPC.
Différentes méthodes ont été utilisées et plusieurs études en rapportent les résultats. Elles ont fait l’objet d’une méta-analyse dans le cadre des Cochrane Reviews en 2004 [14]. Ni le mode de PPC, ni l’humidification systématique ne modifient significativement la durée d’utilisation, même si la préférence des patients semble en faveur des PPC autopilotées. Seules, les interventions éducatives et psychosociales améliorent possiblement l’observance. Ces résultats demandent à être confirmés par des études de plus grande amplitude.
Cependant, le SAOS est une maladie chronique et à ce titre nécessite une prise en charge éducative adaptée (éducation thérapeutique du patient) associant une intelligibilité partagée (nature et mécanisme de la maladie, complications, bénéfices/inconvénients des types de traitement) et la transmission de compétences d’auto-soins (utilisation et gestion du matériel, résolution de problèmes) et psycho-sociales (sentiment d’auto-efficacité, restauration de l’image de soi).
C’est finalement l’association de ces méthodes éducatives aux interventions techniques multiprofessionnelles (prestataires de service, infirmières spécialisées, médecins spécialistes, diététiciennes) qui pourra améliorer l’observance d’un traitement efficace mais contraignant.
Méthodes pour améliorer l’observance du traitement par PPC adapté du Chest [3].
Education thérapeutique du patient.
Implication du conjoint.
Mise en place du traitement au cours d’une hospitalisation dédiée.
Intervention rapide en cas de problème d’interface.
Correction sans délai des effets secondaires.
Communication au patient du relevé d’observance.
Suivi précoce puis régulier par médecin prescripteur et prestataire.
CONCLUSION
La PPC est et demeurera probablement encore quelques années le traitement de référence du SAOS. La fréquence croissante de cette affection dont le diagnostic est encore largement sous estimé, devrait conduire à une augmentation de son utilisation. L’ efficacité de cette thérapeutique sur la somnolence symptôme principal de cette maladie est incontestable. Même si des progrès techniques notables (bruit, encombrement, qualité des interfaces…) ont été accomplis, la tolérance de ce traitement instrumental pose un problème non moins réel chez un nombre important de patients. A la lumière des études effectuées ces progrès ne suffiront pas à en améliorer significativement l’observance.
En attendant qu’un autre traitement du SAOS voit le jour, le défit principal des soignants spécialistes de cette affection envers leurs patients sera de leur faire accepter et supporter la PPC. Une approche multidisciplinaire et interprofessionnelle mêlant interventions techniques et accompagnement éducatif devrait permettre d’atteindre plus facilement cet objectif.
CONFLIT D’INTERÊT
Aucun.
REFERENCES
1. Sullivan CE, Issa FG, Berthon-Jones M, et al. Reversal of obstructive sleep apnea by contunious positive airway pressure applied through the nares. Lancet 1981; 1: 862-865.
2. Robert C, Basner M.D. Continuous Positive Airway Pressure for Obstructive Sleep Apnea. N Engl J Med 2007; 356: 1751-1758.
3. Rahul K., Kakkar anr Richard B. Berry. Positive airway pressure treatement for obstructive sleep apnea. Chest 2007; 132: 1057-2432.
4. Littner M, Hirshkowitz M, Davila D, et al. Standards of practice committee of American academy of sleep medicine practice parameters for the use of autotitrating continuous positive airway pressure devices for titrating pressures and treating adult patients with obstructive sleep apnea syndrome. An American academy of sleep medicine report. Sleep 2002; 1525: 143-147.
5. Sanders MH, Kern N. Obstructive sleep apnea treated by independently adjusted inspiratory and expiratory positive airway pressures via nasal ma sk. Chest 1990; 98: 317-324.
6. Berry RB, Parish JM, Hartse KM. The use of autotitrating CPAP for treatment of adults with obstructive sleep apnea. Sleep 2002; 25: 148-173.
7. Aloia MS, Stanchina M, Arnedt JT, et al. Treatment adherence and outcomes in flexible vs standard continuous positive airway pressure therapy. Chest 2005; 166: 469-473.
8. Teschler H, Dohring J, Wang YM, et al. Adaptative pressure support servo-ventilation: a novel treatment for Cheyne-Stokes respiration in heart failure. Am J Respir Crit Care Med 2001; 164: 614-619.
9. Shneerson J, Wright J. Lifestyle modification for obstructive sleep apnea. (Cochrane review) The Cochrane library. John Wiley and Sons, Chichester 2005; issue 4: 7 pages.
10. Giles TL et coll. Continuous positive airways pressure for obstructive sleep apnea in adults. (Cochrane review) The Cochrane library. John Wiley and Sons, Chichester 2006; issue 4: 8 pages.
11. Rauscher H, Popp W, Wanke T, et al. Acceptance of CPAP therapy for sleep apnea. Chest 1991; 100: 1019-23.
12. Sin DD, Mayers I, Man GCW, et al. Long-term compliance rate to continuous positive airway pressure in obstructive sleep apnea. Chest 2002; 121: 430-435.
13. Laura L. Likar, Toni M Panciera, Allan D. Erickson and Sharon Rounds. Chest 1997; 111:1273-1277.
14. Haniffa M, Lasserson TJ, Smith I. Intervention to improve compliance with continuous positive airway pressure for obstructive sleep apnea. Cochrane Database of Systematic Reviews 2004, issue 4. Art. No.: CD003531. DOI:10.1002/14651858.CD003531.pub2.
TABLES
REFERENCES
1. Sullivan CE, Issa FG, Berthon-Jones M, et al. Reversal of obstructive sleep apnea by contunious positive airway pressure applied through the nares. Lancet 1981; 1: 862-865.
2. Robert C, Basner M.D. Continuous Positive Airway Pressure for Obstructive Sleep Apnea. N Engl J Med 2007; 356: 1751-1758.
3. Rahul K., Kakkar anr Richard B. Berry. Positive airway pressure treatement for obstructive sleep apnea. Chest 2007; 132: 1057-2432.
4. Littner M, Hirshkowitz M, Davila D, et al. Standards of practice committee of American academy of sleep medicine practice parameters for the use of autotitrating continuous positive airway pressure devices for titrating pressures and treating adult patients with obstructive sleep apnea syndrome. An American academy of sleep medicine report. Sleep 2002; 1525: 143-147.
5. Sanders MH, Kern N. Obstructive sleep apnea treated by independently adjusted inspiratory and expiratory positive airway pressures via nasal ma sk. Chest 1990; 98: 317-324.
6. Berry RB, Parish JM, Hartse KM. The use of autotitrating CPAP for treatment of adults with obstructive sleep apnea. Sleep 2002; 25: 148-173.
7. Aloia MS, Stanchina M, Arnedt JT, et al. Treatment adherence and outcomes in flexible vs standard continuous positive airway pressure therapy. Chest 2005; 166: 469-473.
8. Teschler H, Dohring J, Wang YM, et al. Adaptative pressure support servo-ventilation: a novel treatment for Cheyne-Stokes respiration in heart failure. Am J Respir Crit Care Med 2001; 164: 614-619.
9. Shneerson J, Wright J. Lifestyle modification for obstructive sleep apnea. (Cochrane review) The Cochrane library. John Wiley and Sons, Chichester 2005; issue 4: 7 pages.
10. Giles TL et coll. Continuous positive airways pressure for obstructive sleep apnea in adults. (Cochrane review) The Cochrane library. John Wiley and Sons, Chichester 2006; issue 4: 8 pages.
11. Rauscher H, Popp W, Wanke T, et al. Acceptance of CPAP therapy for sleep apnea. Chest 1991; 100: 1019-23.
12. Sin DD, Mayers I, Man GCW, et al. Long-term compliance rate to continuous positive airway pressure in obstructive sleep apnea. Chest 2002; 121: 430-435.
13. Laura L. Likar, Toni M Panciera, Allan D. Erickson and Sharon Rounds. Chest 1997; 111:1273-1277.
14. Haniffa M, Lasserson TJ, Smith I. Intervention to improve compliance with continuous positive airway pressure for obstructive sleep apnea. Cochrane Database of Systematic Reviews 2004, issue 4. Art. No.: CD003531. DOI:10.1002/14651858.CD003531.pub2.
ARTICLE INFO
DOI: 10.12699/jfvp.5.14.2014.18
Conflict of Interest
Non
Date of manuscript receiving
12/02/2014
Date of publication after correction
15/4/2014
Article citation
Baud D. Treatment of sleep apnea syndrome by positive pressure at night. J Func Vent Pulm 2014;05(14):18-24.