
 English
English
 French
French
Pyopneumothorax revealing Boerhaave syndrome
Pyopneumothorax révélant un syndrome de Boerhaave
J.A. Fariña Correa1, K. Boncoungou/Nikièma2, S. Maïga2, A.R. Ouédraogo2, B. Koumbem2, G. Ouédraogo2, G. Badoum/Ouédraogo2, S.M. Ouédraogo1, M. Ouédraogo1
1 : Clinique Edgard Ouédraogo, Ouagadougou, Burkina Faso
2 : CHU Yalgado Ouédraogo Ouagadougou, Burkina Faso
Corresponding author
Dr Maïga Soumaïla
CHU Yalgado Ouédraogo Ouagadougou, Burkina Faso.
Email : maigas01@yahoo.fr
ABSTRACT
The pleuro-digestive fistulas are entities little described in the literature. These are diagnostic and therapeutic emergencies that put the patient's vital prognosis in the short term. We report a case of oesopharyngeal fistula revealed by a left pyopneumothorax in a 58-year-old HIV-positive patient on the second line of treatment.
A triad of signs constitutes Boerhaave syndrome: forceful vomiting, chest pain and subcutaneous emphysema. The syndrome results from spontaneous rupture of oesophageal wall leading to an oeso-pleural or oeso-mediastinal fistula. Positive diagnosis is carried by the esogastric transit to water-soluble substance. Boerhaave's syndrome is a surgical emergency. We report here on a case of spontaneous rupture of the esophagus whose late diagnosis resulted in therapeutic complications but whose clinical management evolved favorably in spite of these complications.
Aerodigestive fistula is a major complication of surgery. BOERHAAVE syndrome, a rare pathology, should be sought in any patient with chest pain with the notion of vomiting. Chest X-ray and oesogastroduodenal transit should be performed urgently in order to quickly establish a diagnosis that guarantees a good prognosis even in PvVIH.
KEYWORDS: Spontaneous rupture; Esophagus; Burkina Faso.
RÉSUMÉ
Les fistules pleuro-digestives sont des entités peu décrites dans la littérature. Il s'agit d'urgences diagnostiques et thérapeutiques mettant en jeu le pronostic vital du patient à court terme. Nous rapportons un cas de fistule œso-pleurale révélée par un pyo-pneumothorax gauche chez un patient de 58 ans, VIH positif en deuxième ligne de traitement.
Le syndrome de Boerhaave, caractérisé par la triade efforts de vomissements, douleurs thoraciques et emphysème sous cutané est du à une brèche spontanée de la paroi oesophagienne entrainant une fistule oeso-pleurale ou oeso-médiastinale. Le diagnostic positif est porté par le transit oesogastrique aux hydrosolubles. Le syndrome de Boerhaave est une urgence chirurgicale. Nous rapportons ici un cas de rupture spontanée de l’œsophage, dont un retard diagnostic a entrainé des complications sur la prise en charge avec cependant une évolution clinique favorable malgré ces complications.
La fistule aérodigestive représente une complication majeure de la chirurgie. Le syndrome de Boerhaave, pathologie rare, doit être recherché devant tout patient présentant une douleur thoracique avec notion de vomissements. Une radiographie thoracique et un transit oeso-gastroduodenal doivent être réalisés en urgence afin de poser rapidement le diagnostic garant d’un bon pronostic même chez le PvVIH.
MOTS CLÉS: Rupture spontanée, oesophage, Burkina Faso.
INTRODUCTION
Les fistules pleuro-digestives sont des entités peu décrites dans la littérature. Il s'agit d'urgences diagnostiques et thérapeutiques mettant en jeu le pronostic vital du patient à court terme. Nous rapportons un cas de fistule œso-pleurale révélée par un pyo-pneumothorax gauche chez un patient de 58 ans, VIH positif en deuxième ligne de traitement.
OBSERVATION
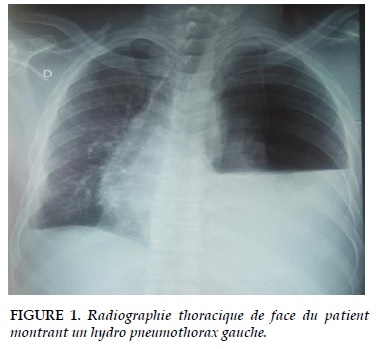
Le patient K O, 58ans, économiste de profession, a été reçu à la clinique Edgard Ouedraogo (Ouagadougou) le 28 décembre 2017 pour dyspnée, fébrile avec douleur hémi-thoracique gauche aigue sur fond d’altération progressive de l’état général depuis septembre 2017. Il avait été traité pour syndrome palustre 15 jours auparavant. L’examen révèle un syndrome d’épanchement pleural mixte gauche de grande abondance (Figure 1) confirmé par une ponction exploratrice qui ramène un liquide purulent, fétide.
Ses antécédents sont marqués par une tuberculose pulmonaire traitée et déclarée guérie en 2002, une infection par le VIH découverte en 2002 sous deuxième ligne de traitement (non observant pour les ARV) et un tabagisme (3PA) sevré, y compris une consommation excessive et régulière d’alcool.
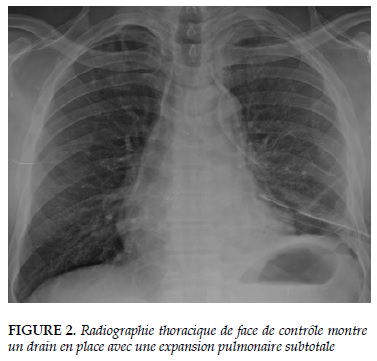
A l’admission, l’état général était altéré avec sepsis et saturation à 89% à l’air ambiant. Un drain thoracique a été posé avec réanimation classique et une antibiothérapie probabiliste à base d’amoxicilline+acide clavulanique 3g par 24 heures, métronidazole injectable 1,5 g par 24 heures. La radiographie thoracique de contrôle (Figure 2) montre un drain en place avec une expansion pulmonaire subtotale. La culture du pus pleurale a isolé Aeromonas hydrophila et Candida ablicans. L’antibiothérapie a été immédiatement adaptée aux tests de sensibilité et le patient mis sous fluconazole injectable, ceftazidime et conservation de l’imidazole. Les hémocultures de même que la recherche de BAAR dans le pus ont été négatives. Le dosage des CD4 est revenu à 65 cellules/mL.
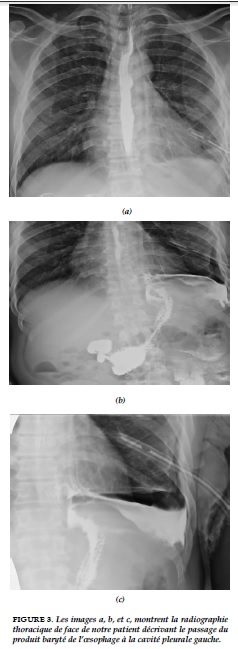
Au 7ème jour de drainage, la clarification des sécrétions et la disparition de la fétidité contrastaient avec l’abondance des sécrétions qui sont restées abondantes depuis la mise en place du drain thoracique, ramenant entre 1,5 à 2 litres par jour. Au 9ème jour de drainage une constatation de débris alimentaires est rendue possible par un liquide pleural de plus en plus clair. Un transit œsogastrique baryté a été réalisé dès le lendemain (J10) objectivant un passage du produit baryté de l’œsophage à la cavité pleurale gauche (Figure 3).
Une thoracotomie exploratrice postéro-latérale gauche a permis d’objectiver une perforation d’environ 1 cm au tiers inferieur de l’œsophage avec un important sepsis intra thoracique avec une grande quantité de dépôt de fibrine. Le diagnostic de fistule œso-pleurale gauche a été retenu, réparée et un drain thoracique de nouveau mis en place. L’alimentation per os a été remplacée par une alimentation parentérale par voie centrale.
Cependant au 15ème jour après la thoracotomie, un transit baryté a objectivé à nouveau un passage du produit baryté de l’œsophage à la cavité pleurale gauche. Le patient a bénéficié d’une thoraco-laparotomie qui a mis en évidence un lâchage partiel de l’ancienne suture qui a été reprise suivie d’une gastrotomie d’alimentation et ceci a également permis la reprise également des ARV, qui avait été suspendu au décours de la première thoracotomie. Les suites opératoires ont été simples. La constatation d’une dépression a nécessité une prise en charge psychologique. Le patient est sorti 40 jours après son admission le 6 Février 2018. Une visite contrôle réalisée, a constaté une amélioration clinique et radiographique.
DISCUSSION
Les fistules œso-pleurales peuvent être cervicales, thoraciques hautes au niveau de la crosse aortique vasculaires ou basses [1]. Le plus souvent, elles sont post-traumatiques ou d’origine iatrogène survenant lors d’une tentative d’intubation ou d’une endoscopie digestive (oesophagoscopie), après une pneumonectomie, ou encore après une lobectomie où le délai d’apparition varie de 6 jours à 2 mois. Ces fistules peuvent être rarement occasionnées par une rupture spontanée de l’œsophage (RSO) connue sous le nom de syndrome de Boerhaave en référence au scientifique qui a décrivit le phénomène pour la première fois en 1724 avant d’être repris par Barret en 1946 [2]. La forme la plus fréquente de fistules thoraciques est broncho pleurale [3]. Cependant d’autres types de fistules sont décrites dans la littérature notamment les fistules broncho-œsophagiennes et broncho bronchique [3,4].
Le syndrome de Boerhaave est caractérisé par la triade: efforts de vomissements, douleur thoracique et emphysème sous cutané, correspondant à une rupture du tiers inferieur de l’œsophage [5] comme ce fut dans notre cas. C’est une pathologie rare, de diagnostic difficile et dont le pronostic dépend de la précocité de la prise en charge. Cette RSO concerne principalement l’homme (80% des cas), avec un âge moyen de survenue entre 40 et 60 ans [5,6]. La mortalité est variable selon les études, mais va de 28% à 85% en fonction du délai de la prise en charge [7]. Cette RSO survient le plus souvent à la suite d’un effort de vomissements qui entraine une augmentation soudaine de la pression intra thoracique ou intra abdominale, transmise à un œsophage mal relaxé et /ou dont l’extrémité supérieure est occluse [8]. Le tableau clinique varie mais est souvent dominé par la douleur thoracique et/ou abdominale orientant le diagnostic surtout si elle survient après un effort de vomissement. La triade pathognomonique caractérisant ce syndrome n’est que rarement retrouvée.
L’examen de référence permettant de confirmer le diagnostic s’il est réalisé avant la 48ème heure, est le scanner thoracique avec opacification de l’œsophage qui supplante le transit œsophagien à la gastrographine [9]. Cependant le transit œsogastroduodenal à la gastrographine, examen largement disponible et peu onéreux, garde toute son importance dans les pays à faible revenu et où l’assurance maladie universelle n’est pas encore effective. En effet, ces deux examens contribuent à poser le diagnostic en permettant de visualiser l’extravasation du produit de contraste par la brèche œsophagienne. La radiographie thoracique peut mettre en évidence un pneumo-médiastin ou un hydro-pneumothorax comme ce fut le cas de notre patient, orientant le diagnostic [5].
Le pronostic de cette pathologie dépend de la rapidité de la prise en charge. Les premières 24 heures sont déterminantes, tout retard au diagnostic augmentant de façon notable la mortalité qui peut atteindre 100% [10]. Le traitement doit être initié le plus rapidement possible pour juguler l’évolution vers la défaillance cardiorespiratoire et l’installation d’un tableau septique. Il reste le plus souvent chirurgical et ce d’autant plus que le diagnostic est précoce. Cette prise en charge chirurgicale consiste en une suture des berges de la rupture œsophagienne [11]. Si l’intervention est réalisée au delà des 12 premières heures, un risque de désunion des berges est possible par nécrose des bords de la rupture, de l’oedème localisé et du milieu septique comme ce fut le cas de notre patient, qui a été repris au bloc après un lâchage du fil de la première intervention.
Nous avons isolé, dans le produit pathologique pleural de notre patient inobservant au traitement ARV de 2ème ligne, Aeromonas hydrophila et Candida ablicans. Si nous ne pouvons être formels sur la responsabilité de ces germes dans la genèse de cette fistule, il reste que des causes infectieuses et parasitaires sont reconnues dans la survenue de fistules thoraciques. En effet, la prévalence d’une fistule chez les patients atteints d’une tuberculose varie de 10 à 50 % et se normalise après le traitement antituberculeux [12]. Cependant, des fistules broncho-médiastinales causées par l’infection à Aspergillus fumigatus, ont été décrites [13].
Si sa prise en charge reste chirurgicale, un traitement médicamenteux trouve souvent son indication surtout en cas de petites fistules ou d’étiologies infectieuses. L’évolution a été favorable chez notre patient, malgré la reprise de l’intervention chirurgicale. A noter que notre prise en charge fut globale avec l’instauration d’une psychothérapie permettant la reprise de son traitement ARV chez ce patient qui était inobservant bien qu’il fût sous ce traitement depuis 2002. Il est probable que la complétude du traitement ARV, rendue possible par la gartrostomie réalisée lors de la deuxième intervention, a contribué à l’amélioration du pronostic chez notre patient.
CONCLUSION
La fistule aérodigestive représente une complication majeure de la chirurgie. Le syndrome de Boerhaave, pathologie rare, doit être recherché devant tout patient présentant une douleur thoracique avec notion de vomissements. Une radiographie thoracique et un transit oeso-gastroduodenal doivent être réalisés en urgence afin de poser rapidement le diagnostic garant d’un bon pronostic même chez le PvVIH.
CONFLIT D’INTERETS
Les auteurs déclarent ne pas avoir de liens d’intérêts.
RÉFÉRENCES
1. Ribet M. Traumatismes de l’oesophage. Encycl. Méd. Chir. (Paris) 9203 A-10.
2. Detrierp H. Chirurgie d’urgence. Plaie et rupture de l’oesophage. Masson, Ed. Paris, 1976, 253-265.
3. Nemati A, Safavi E, Ghasemiesfe M, Anaraki MZ, Firoozbakhsh S, Khalilzadeh O, et al. Fistula for-mation between the right and left main bronchus caused by endobronchial tuberculosis. Am J Med Sci 2012; 343:330-1.
4. Madan K, Venkatnarayan K, Shalimar, Mohan A. Successful medical management of tuberculous bron-cho-oesophageal fistula. BMJ Case Rep 2014. doi:10.1136/bcr-2013-202560
5. Rissoan C, Louerat C, Riou R, Lantheaume S. Syn-drome de Boerhaave et grossesse. A propos d’un cas et revue de la littérature. Jour Gyn Obste et Biol Re-produc, 2009 ; 38, 250-3.
6. Dayen C, Mishellany H, Hellmuth D, Mayeux I, Au-bry P, Glerant JC et al. La rupture de l’oesophage ou syndrome de Boerhaave. A propos de trois cas et re-vue de la littérature. Rev Mal Respir , 2001, 18, 537-40.
7. Sache L, Piot P, Delin C, Tavernier D, Feuchere P, Faitg R : Perforation spontanée de l’oesophage : une urgence chirurgicale. Rean Urg 1996 ; 5 : 417-9
8. Tidman MK, John HT : spontaneous rupture of the oesophagus. Brit J Surg 1967 ; 4 : 286-92.
9. Newcomb AE, Clarke CP. Spontaneous pneumomedi-astinum : a benign curiosity or a significant problem ? Chest 2005 ; 128 :3298-302.
10. Lauwrence Dr, Ohri SK, Moxon RE, Townsend ER, Fountain SW. Primary oesophageal repair for Boer-haave’s syndrome. Ann Thorac Surg 1999 ; 67 : 818-20.
11. Shenfine J, Dressner SM, Vishwanat Y, Hayes N, Grif-fin SM. Management of spontaneous Pneumome-diastinum : 41 cases. Eur J Cardiothorac Surg 2007 ; 31 :1110-4
12. Kim M, Kang ES, Park JY, Kang HR, Kim JH, Chang Y, et al. Fistula formation between right upper bronchus and bronchus interme- dius caused by endobronchial tuberculosis: a case report. Tuberc Respir Dis 2015;78:286-8.
13. Lettre à la rédaction. Une fistule endobronchique fai-sant découvrir une tuberculose : une présentation aty-pique en France. Revue de Pneumologie clinique 2017; 73, 276-9.
FIGURES
RÉFÉRENCES
1. Ribet M. Traumatismes de l’oesophage. Encycl. Méd. Chir. (Paris) 9203 A-10.
2. Detrierp H. Chirurgie d’urgence. Plaie et rupture de l’oesophage. Masson, Ed. Paris, 1976, 253-265.
3. Nemati A, Safavi E, Ghasemiesfe M, Anaraki MZ, Firoozbakhsh S, Khalilzadeh O, et al. Fistula for-mation between the right and left main bronchus caused by endobronchial tuberculosis. Am J Med Sci 2012; 343:330-1.
4. Madan K, Venkatnarayan K, Shalimar, Mohan A. Successful medical management of tuberculous bron-cho-oesophageal fistula. BMJ Case Rep 2014. doi:10.1136/bcr-2013-202560
5. Rissoan C, Louerat C, Riou R, Lantheaume S. Syn-drome de Boerhaave et grossesse. A propos d’un cas et revue de la littérature. Jour Gyn Obste et Biol Re-produc, 2009 ; 38, 250-3.
6. Dayen C, Mishellany H, Hellmuth D, Mayeux I, Au-bry P, Glerant JC et al. La rupture de l’oesophage ou syndrome de Boerhaave. A propos de trois cas et re-vue de la littérature. Rev Mal Respir , 2001, 18, 537-40.
7. Sache L, Piot P, Delin C, Tavernier D, Feuchere P, Faitg R : Perforation spontanée de l’oesophage : une urgence chirurgicale. Rean Urg 1996 ; 5 : 417-9
8. Tidman MK, John HT : spontaneous rupture of the oesophagus. Brit J Surg 1967 ; 4 : 286-92.
9. Newcomb AE, Clarke CP. Spontaneous pneumomedi-astinum : a benign curiosity or a significant problem ? Chest 2005 ; 128 :3298-302.
10. Lauwrence Dr, Ohri SK, Moxon RE, Townsend ER, Fountain SW. Primary oesophageal repair for Boer-haave’s syndrome. Ann Thorac Surg 1999 ; 67 : 818-20.
11. Shenfine J, Dressner SM, Vishwanat Y, Hayes N, Grif-fin SM. Management of spontaneous Pneumome-diastinum : 41 cases. Eur J Cardiothorac Surg 2007 ; 31 :1110-4
12. Kim M, Kang ES, Park JY, Kang HR, Kim JH, Chang Y, et al. Fistula formation between right upper bronchus and bronchus interme- dius caused by endobronchial tuberculosis: a case report. Tuberc Respir Dis 2015;78:286-8.
13. Lettre à la rédaction. Une fistule endobronchique fai-sant découvrir une tuberculose : une présentation aty-pique en France. Revue de Pneumologie clinique 2017; 73, 276-9.
ARTICLE INFO
DOI: 10.12699/jfvpulm.9.27.2018.42
Conflict of Interest
Non
Date of manuscript receiving
03/07/2018
Date of publication after correction
31/08/2018
Article citation
Fariña Correa J.A, Boncoungou/Nikièma K, Maïga S, Ouédraogo A.R, Koumbem B, Ouédraogo G, Badoum/Ouédraogo G, Ouédraogo S.M, Ouédraogo M. Pyopneumothorax revealing Boerhaave syndrome. J Func Vent Pulm 2018;27(9):42-45.